Virus de la fièvre jaune — Wikipédia
| Domaine | Riboviria |
|---|---|
| Famille | Flaviviridae |
| Genre | Flavivirus |
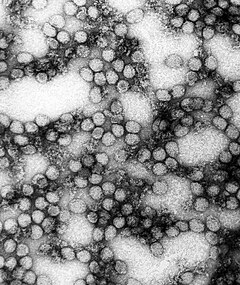
Le virus de la fièvre jaune, ou virus amaril, est l'agent infectieux qui, chez l'homme, provoque la fièvre jaune. Ce flavivirus est le premier à avoir été isolé, à la fin des années 1920. Il s'agit d'un virus à ARN monocaténaire de polarité positive, appartenant donc au groupe IV de la classification Baltimore. Le vecteur de ce virus est un moustique du genre Aedes en Afrique ou Haemagogus (en) en Amérique du sud.
Qu’est-ce que la fièvre jaune ?[modifier | modifier le code]
La fièvre jaune est une hépato-néphrite[2] pouvant évoluer vers un syndrome hémorragique.
Comme son nom l’indique, cette infection est caractérisée par un ictère, résultant de lésions nécrosantes du foie. De plus, cette infection peut causer des lésions rénales et cardiaques ainsi que des saignements de la muqueuse digestive pouvant entraîner une hématémèse et un méléna. La fièvre jaune est l’infection à arbovirus la plus importante en termes de létalité.
Elle a son origine en Afrique, car l’humidité de la forêt de l’Afrique de l’Ouest favorise le développement des moustiques réservoir de la fièvre jaune. C’est le moustique vecteur Aedes aegypti qui le propage vers le Nouveau Monde durant le XVIIe siècle par les bateaux à voile et le commerce d’esclaves.
Classification et structure[modifier | modifier le code]
Le virus de la fièvre jaune est du genre Flavivirus, faisant partie de la famille des Flaviviridae. Cette particule virale était anciennement classée avec les Togaviridae.
Il y a quelque temps, les flavivirus étaient regroupés sous le terme anglo-saxon d’arbovirus de groupe B (« Arthropode borne virus », virus transmis par les arthropodes).
Le Flavivirus est un petit virus d’environ 40 nm de diamètre. Il démontre un génome à ARN monocaténaire de polarité positive d’environ 11-12 kb. Il est coiffé en 5’ et porte une séquence poly A en 3’. Sa capside est icosaédrique.
Le virus de la fièvre jaune est un virus enveloppé. Les virus enveloppés sont beaucoup plus fragiles que les virus nus (non enveloppés). Les flavivirus sont donc sensibles aux solvants des graisses tels : l’éther et le désoxycholate de sodium. De plus, l’enveloppe virale porte des spicules HA (Cette HA est active sur les globules rouges d’oiseaux) elles ont une activité hémagglutinante.
Les protéines codées sont E (enveloppe), M (protéines de membrane), C (Protéines de capside) et NS (protéines non-structurales). Grâce à ces protéines, le virus est capable d’infecter et de se répliquer dans une cellule hôte.
Origines géographiques[modifier | modifier le code]
Le virus de la fièvre jaune fut isolé en Amérique en 1927 et en Afrique en 1928[3].
Le virus de la fièvre jaune est absent en Asie, pour des raisons qui restent inexpliquées. Au début, on pensait que c’était dû à la présence du virus de la dengue (qui apporterait une protection croisée), mais on s’est rendu compte que dans certains pays ils pouvaient coexister ensemble.
Les grandes zones géographiques touchées par la fièvre jaune sont l’Afrique et l’Amérique du Sud (Venezuela, Colombie, Guyane, Guyana, Surinam, Brésil et certaines îles des Caraïbes)[4].
En 1944, on a constaté que le virus pouvait provoquer, en Amérique du sud, une très forte mortalité chez les singes, comme le marmouset. Alors qu'en Afrique, les singes africains ne font qu'une infection inapparente, suivie d'une immunité durable. On sait aussi que la fièvre jaune de jungle est moins grave que la fièvre jaune en zone urbaine qui peut s’avérer mortelle.
De nos jours, on peut séquencer les différentes souches virales. Pour ce faire, on utilise la région codant les protéines E et NS1 du virus, ou l’extrémité 3’ non codante de l’ARN. On utilise environ 11 000 bases. Le choix de ces régions dépend de leur association à des fonctions virales importantes telles la virulence, la reconnaissance du récepteur cellulaire et la fixation d’anticorps neutralisants. La comparaison entre les séquences permet la création d’un arbre phylogénétique déterminant les origines et les relations entre souches viralesl[5], ainsi que la distinction entre virus sauvages et virus atténués vaccinaux[6].
En 2008, on distingue au moins 7 génotypes distincts d'origine géographique différente. Les souches africaines sont au nombre de 5 : Afrique de l'Ouest type I et II qui se distinguent de Centre-Afrique, Angola et Afrique de l'Est, par des vecteurs différents (espèces de moustiques). Il existe une faible différence entre les souches africaines de l'ouest et les américaines[7].
Ces études sont en faveur de l'origine africaine du virus de la fièvre jaune, la souche africaine de l'est étant la plus ancienne, divergeant d'un flavivirus ancestral, il y a 1500 à 3000 ans[8]. Puis les souches africaines de l'ouest ont divergé de celle de l'est, 300 ans avant l'introduction du virus aux Amériques par le commerce des esclaves. La souche américaine est ainsi plus proche de souches africaines de l'ouest que ces dernières ne le sont des souches de l'est[7].
Mode de transmission et évolution de la fièvre jaune[modifier | modifier le code]
Dans la fièvre jaune sylvatique, l'homme se contamine lors des activités forestières (abattage d’arbres par exemple), lorsque les moustiques y prolifèrent à la saison des pluies. Les singes jouant le rôle d'amplificateur (singe - moustique - homme).
Dans la fièvre jaune urbaine, les moustiques anthropophiles (piquant préférentiellement l'homme) prennent le relais, l'homme jouant le rôle d'amplificateur (homme - moustique - homme).
Mode de réplication[modifier | modifier le code]
Chez le moustique, la réplication du virus amaril se fait au niveau du tube digestif, des organes reproducteurs et des glandes salivaires du moustique, après fusion avec la membrane cellulaire et pénétration directe dans les cellules. Il faut 7 à 10 jours entre l'ingestion de sang infecté et la sécrétion virale dans la salive du moustique. L'infection des organes reproducteurs expliquent une transmission dite verticale (des femelles fécondées à leurs propres œufs ou transmission trans-ovarienne) et une autre dite horizontale (des mâles congénitalement infectés aux femelles lors de l'accouplement). Ceci explique que les moustiques ne jouent pas seulement un rôle de vecteur, mais qu'ils constituent aussi le réservoir naturel du virus de la fièvre jaune[9].
Chez l'hôte vertébré (primates), après une piqûre, le virus se lie aux récepteurs cellulaires (non identifiés en 2008) et entre par endocytose. Le génome, dans ce cas l’ARN monocaténaire, est libéré dans le cytoplasme de la cellule par fusion, sous l’effet du pH acide des phagolysosomes. La réplication a lieu exclusivement dans le cytoplasme. La majorité du génome est directement traduite en une polyprotéine à partir de son extrémité 5'. La polyprotéine est ensuite clivée en 4 protéines virales non structurales, qui sont l’ARN polymérase, une protéase, une hélicase ainsi qu'une enzyme de méthylation et de capping. Le brin complémentaire de polarité négative est synthétisé grâce à ces enzymes virales. Ensuite un brin complet de polarité positive est transcrit; de plus, un ARN subgénomique est synthétisé. Celui-ci code une polyprotéine qui est clivée pour produire des protéines structurales, la nucléocapside( C ), les glycoprotéines de surface (E1 et E2) et une protéine transmembranaire.
L’assemblage du virus débute donc dans le cytoplasme et se termine dans la membrane plasmique par l’incorporation des glycoprotéines virales de surface contenant des lipides. C'est ainsi que les virions sont relargués à l'extérieur de la cellule et prêts pour en contaminer d'autres cellules.
Diagnostic[modifier | modifier le code]
On peut conserver le virus à −80 °C ou lyophilisé.
On utilise plusieurs techniques afin de mettre en évidence les flavivirus:
- Sérologie : Normalement, on cherche des anticorps qui ont la capacité de dévier le complément, qui inhibent l’hemagglutination et neutralisants.
- Inhibition des foyers fluorescents en cultures cellulaires - ELISA (grâce à la détection des IgM antiamariles en immunocapture)
- Culture virale : Le virus de la fièvre jaune est cultivable sur cellules VERO, PS2 (rein de proc) et Aedes albopictus (cellules de moustiques).
- Biologie moléculaire
Prévention et traitement[modifier | modifier le code]
Il n’y a pas de traitement curatif, il faut donc prévenir. Pour ce faire, on peut[2] :
- S’informer sur les risques endémiques.
- Déclaration des cas de fièvre jaune à l’OMS.
- Démoustication.
- Vaccination : Une vaccination efficace contre la fièvre jaune est apparue en 1930 aux États-Unis (Theiler et Smith) et en Afrique à Dakar en 1932 (Sellards et Laigret). Depuis les années 1980, seul le vaccin de Theiler est utilisé dans le monde (souches virales atténuées : soit 17 D, soit 17D204).
Notes et références[modifier | modifier le code]
- (en) « Virus Taxonomy: 2018b Release », ICTV, (consulté le ).
- [PDF] La fièvre jaune, article de em-consulte lire en ligne
- H.J.A. Fleury, Virologie humaine : Abreges, Paris, Masson, , 2e éd., 195 p. (ISBN 2-225-82969-1)
- H.J.A. Fleury, Virologie humaine : connaissances et pratique, Paris, Masson, , 4e éd., 245 p. (ISBN 2-294-00815-4)
- H. Tolou, M-R. Pisano et J-P. Durand, Les maladies quarantenaires : Epidemiologie moleculaire de la fièvre jaune, vol. 58, t. supplément 2, France,
- (en) T.P. Monath, M.S. Cetron et D.E. Teuwen, Yellow fever vaccine, Philadelphie, Saunders Elsevier, , 1725 p. (ISBN 978-1-4160-3611-1, lire en ligne), p. 974Dans Vaccines, S. Plotkin, 5e édition.
- T.P. Monath et coll. 2008, op. cit, p.976-978.
- T.P. Monath et coll. 2008, op. cit, p.959.
- T.P. Monath et coll. 2008, op. cit, p.967-968.
Annexes[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
(en) Bernard N. Fields et David M.Knipe, Fields Virology, vol. 1, New York, Raven Press New York, , 1267 p.
(en) David M. Knipe et Peter M. Howley, Fields Virology, Philadelphie, Lippincott Williams & Wilkins, , 4e éd., 1579 p. (ISBN 0-7817-1832-5)
(en) James H. Strauss et Ellen G. Strauss, Viruses and human disease, USA, Elsevier, , 2e éd., 468 p. (ISBN 978-0-12-373741-0)
(en) Brian W.J. Mahy et Volker Ter Meulen, Topley & Wilson's microbiology & microbial infections : Virology, vol. 2, Washington, Hodder Arnold, 10e éd., 1759 p. (ISBN 978-0-340-88562-8 et 0-340-88562-9)
Leslie Collier et John Oxford, Virologie humaine : De la biologie à la clinique, Paris, Médecine-Sciences Flammarion, , 284 p. (ISBN 2-257-11343-8)
Pierre Lépine, Les virus, France, Presses universitaires de France, , 1re éd., 124 p.


 French
French Deutsch
Deutsch