Малеїнова кислота — Вікіпедія
| Малеїнова кислота | |
|---|---|
 | |
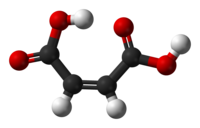 | |
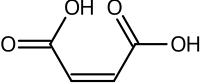
| Назва за IUPAC | цис-бутен-2-діова кислота |
| Ідентифікатори | |
| Номер CAS | 110-16-7 |
| Номер EINECS | 203-742-5 |
| DrugBank | 04299 |
| KEGG | C01384 |
| ChEBI | 18300 |
| RTECS | OM9625000 |
| SMILES | C(=CC(=O)O)C(=O)O[1] |
| InChI | InChI=1S/C4H4O4/c5-3(6)1-2-4(7)8/h1-2H,(H,5,6)(H,7,8)/b2-1- |
| Номер Бельштейна | 605762 |
| Номер Гмеліна | 49854 |
| Властивості | |
| Молекулярна формула | C4H4O4 |
| Молярна маса | 116,073 г/моль |
| Густина | 1,5902 г/см³[2] |
| Тпл | 139 °C |
| Розчинність (вода) | 44,1 % |
| Розчинність (бензен) | 0,024 % |
| Кислотність (pKa) | 1,92 6,23 |
| Дипольний момент | 10,6 |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 | -789,4 кДж/моль (тв.) |
| Теплоємність, c p | 137,0 Дж/(моль·K) (тв.) |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Малеї́нова кислота́, цис-2-буте́ндіо́ва кислота́ — двоосновна ненасичена карбонова кислота. Разом зі своїм транс-ізомером, фумаровою кислотою, малеїнова є найпростішим представником цього ряду сполук.

За звичайних умов речовина є білою порошкоподібною речовиною. Вона має добру розчинність у воді, що дозволяє проводити розділення її суміші із фумаровою кислотою шляхом кристалізації.
Отримання[ред. | ред. код]
Основним способом синтезу кислоти є взаємодія малеїнового ангідриду, отриманого окисненням бензену, із невеликою кількістю води:
Окрім цього типовим способом отримання малеїнової кислоти (а також і фумарової) є дегідратація яблучної кислоти за нагрівання:
Хімічні властивості[ред. | ред. код]
При нагріванні із сильними осушниками (оцтовим ангідридом, фосфорним ангідридом) кислота втрачає воду й утворює малеїновий ангідрид.
За тривалого нагрівання до 150 °C або при ультрафіолетовому опромінюванні відбувається ізомеризація:
На прикладі цієї реакції Йоганнес Вісліценус у 1877 році відкрив передбачену Вант-Гоффом цис-транс-ізомерію для сполук із подвійним зв'язком.
Подвійний зв'язок у сполуці легко відновлюється при дії амальгами натрію із утворенням відповідної насиченої бурштинової кислоти.
Малеїнова кислота є двоосновною: константа кислотної дисоціації за першим ступенем становить 1,92 і 6,23 для другого ступеня.
Примітки[ред. | ред. код]
| Вікісховище має мультимедійні дані за темою: Малеїнова кислота |
Джерела[ред. | ред. код]
- CRC Handbook of Chemistry and Physics / Lide, D. R., editor. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Lohbeck K., Haferkorn H., Fuhrmann W. Maleic and Fumaric Acids // Ullmann's Encyclopedia of Industrial Chemistry. — 6th. — Weinheim : Wiley-VCH, 2005. — P. 1—2. — DOI: (англ.)
- Чирва В. Я., Ярмолюк С. М., Толкачова Н. В., Земляков О. Є. Органічна хімія. — Львів : БаК, 2009. — С. 554—555. — ISBN 966-7065-87-4.
- Гауптман З., Грефе Ю., Ремане Х. Органическая химия / Пер. с нем. под ред. В. М. Потапова. — М. : Химия, 1979. — С. 434—435. (рос.)
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


 French
French Deutsch
Deutsch

