Alkol - Vikipedi
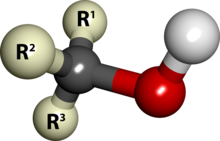
Alkol, karbon atomuna doğrudan bir -OH (hidroksil) grubunun bağlı olduğu organik bileşiklere verilen genel ad. Genel formülü CnH2n+1OH olan mono alkoller, alkollerin önemli bir sınıfıdır. Bunlardan etanol (C2H5OH), alkollü içeceklerde bulunan türüdür. Genellikle alkol kelimesi ile etanol kastedilir ki yeni fermente olmuş birada etanol oranı %3-5 arasında iken şarapta %12-15 arasındadır.[1]
Etimoloji[değiştir | kaynağı değiştir]
Türkçeye Fransızca alcool sözcüğünden geçen[2] alkolün kökeni Arapça al-kuhl (kara toz) sözcüğüdür.[3] Arapçada kuhl denen madde sürme yapımında kullanılan antimon sülfat ve kurşun sülfattır.[3]

Kimyasal yapılarına göre alkoller[değiştir | kaynağı değiştir]
Alifatik alkoller[değiştir | kaynağı değiştir]
Mono alkoller[değiştir | kaynağı değiştir]
Doymuş hidrokarbonlarlardan türemiş olanların genel formülü CnH2n+1-OH (R-OH) şeklindedir. Bir alkil (R) grubuna bir -OH grubunun bağlanmasıyla teşekkül etmektedirler. Mono alkoller üç ayrı sınıfta toplanır:
- Primer (birincil) alkoller: -OH grubu bir uçtaki karbona bağlı olup bu karbona en az iki H atomu bağlı olur. CH3 -CH2-OH gibi.
- Sekonder (ikincil) alkoller: -OH grubu aradaki herhangi bir karbona bağlı olan alkollerdir. -OH grubunun bağlı olduğu karbona bir H atomu bağlı olur. CH3-CHOH-CH3 gibi.
- Tersiyer (üçüncül) alkoller: -OH grubu H’sı olmayan karbona bağlıdır. (CH3)3COH gibi.
Mono alkollerin adlandırılması[değiştir | kaynağı değiştir]
Türediği parafinin sonuna -ol eki veya alkilin isminden sonra “alkol” kelimesi getirilerek adlandırılırlar:
- CH3-OH metanol (metil alkol)
- C2H5-OH etanol (etil alkol)
- C3H7-OH propanol (propil alkol)
- C4H9-OH bütanol (bütil alkol)
Dört karbonlu bir alkol primer, sekonder veya tersiyer olabilir. Farkı belirtebilmek için -ol ekinden önce -OH grubunun bağlı olduğu karbonun numarası söylenmelidir:
CH3-CH2-CH2-CH2-OH Bütan-1-ol (primer)
CH3-CH2-CHOH-CH3 Bütan-2-ol (sekonder)
Metil alkol (Metanol, Karbinol): CH3OH[değiştir | kaynağı değiştir]
Saf metanol 64,7 derecede kaynayan renksiz ve akışkan bir sıvı olup, parlak olmayan mavimsi bir alevle yanar. Bütün organik çözücüler de ve suda her oranda çözünür. Metanol ilk defa 1661’de odunun kuru kuruya damıtılmasıyla saf hâlde elde edildi. Damıtma ürününde % 1,5-3 metanol, % 10 asetik asit, % 0,5 aseton ve başkaları bulunmaktadır. Endüstride çözücü ve motor yakıtlarının bir bileşeni olarak geniş çapta kullanılır. Formaldehit ve anilin boyalarının elde edilişinde kullanılır. Ayrıca metillendirme vasıtası olarak organik sentezlerde ve tıbbı ve endüstriyel etanolün içilmezliğini sağlamada yaygın olarak kullanılır.
Endüstride, karbonmonoksit ile hidrojenin reaksiyonundan elde edilir. Bu metodla saf metanol elde edilirse de sıcaklığın 30-40 derece yükselmesi hâlinde n- propanol ve izobütanol teşekkül edebilir. Fraksiyonlu destilasyonla sulu çözeltisinden %99’luk bir saflıkta elde edilir. Susuz (mutlak) metanol elde etmek için Mg kullanılır:
- 2 CH3OH + Mg → (CH3O)2Mg + H2
- (CH3O)2Mg + H2O → 2C H3OH + MgO
Çok az miktardaki metanol canlı organizma için zehirlidir. Kalıcı bozukluklar meydana getirir. Örneğin 25 gram metanol içilirse körlüğe sebep olur.
Etil alkol (Etanol) C2H5OH[değiştir | kaynağı değiştir]
Etanol, renksiz ve yanıcı bir sıvıdır. İçkilerde bulunan alkol türüdür ve tüketilmesi sarhoşluğa sebep olur. Metil alkol zehirlenmelerinde panzehir olarak da kullanılır. Sanayideki etil alkolün üretimi etan gazının sülfürik asit eşliğinde suyun içinde çözülmesiyledir.
CH2=CH2+H2O → CH3-CH2-OH
Propil alkoller (Propanoller): C3H7OH[değiştir | kaynağı değiştir]
İki tane yapı izomeri vardır; n-propanol ve izopropanol. n-propanol, CH3-CH2-CH2-OH hoş kokulu, renksiz, 97.2 derecede kaynayan bir sıvıdır. Metanol sentezi yanında bir yan ürün olarak ve füzel yağı içinde bulunur. Ticari olarak oxo prosesi denilen işlemle hazırlanır. İzopropanol, (CH3)2-CH-OH, 82.4 derecede kaynayan renksiz bir sıvıdır. Asetonun katalitik hidrojenasyonu ile elde edilebilir. Ticari olarak propenin sülfürik asit içinde tutulması ve bunu müteakip meydana gelen esterin hidrolizi ile elde edilir.
Propanol ve izopropanol çözücü olarak sık kullanılır.
Poli alkoller (Polioller)[değiştir | kaynağı değiştir]
Bu sınıf bileşikleri temsil eden en basit örnekler, dihidrik alkol etilen glikol ve propilen glikol, trihidrik alkol gliserin ve tetrahidrik alkol eritritoldür:
- CH2OH-CH2OH (Etilen glikol)
- CH2OH-CHOH-CH2-OH (Gliserin)
- CH2OH-CHOH-CHOH-CH2OH (Eritritol)
Bu bileşiklerin hidroksil grubu arttıkça dietil eter ve etanoldeki çözünürlükleri artar. Polialkollerin bazısı kıymetli tabii ürünlerin birer bileşenidir. Mesela gliserin yağlarda bulunur. Daha yüksek polialkoller mesela pentiol ve hekzitoller karbonhidratlar kimyasında önemli yer tutar.
Etilen glikol[değiştir | kaynağı değiştir]
Etilen glikol renksiz, kaynama noktası 198 derece olan viskoz (kıvamlı) tatlımsı bir yağdır. Su ve alkolde her oranda karışır, 1,2-glikollerin kimyasal özellikleri mono alkollerinkine benzer. Etilen glikolün biraz derişik sülfürik asitle veya derişik fosforik asitle ısıtılmasıyla önemli bir çözücü olan dioksan elde edilir.
Elde edilişi:
- Mono alkollere benzer olarak 1,2-dihalojen alkanlardan sulu potasyum hidroksit veya alkol metal karbonat yardımıyla hidrolizle elde edilebilir. Misal 1,2-dibromoetan, etilen glikol verir.
- Etilen glikol endüstriyel olarak etilenden aşağıdaki metodlarla elde edilir:
- Etilen, klorlu sudan geçirilir. Meydana gelen etilen klorohidrin sodyum bikarbonat sulu çözeltisiyle hidroliz edilir.
- Etilen oksitin soğuk, sulandırılmış hidroklorik asitle muamalesiyle elde edilir.
Kullanılışı: Etilen glikol, onun monometil eteri, monoetil eteri ve dioksan önemli çözücüdürler. (Misal, vernikler ve selüloz asetatlar için.) Etilen glikol antifriz olarak, gliserin yerine sık sık kullanılır.
Gliserin[değiştir | kaynağı değiştir]
Gliserin, poli alkollerin en önemlisi ve hemen hemen hayvanî ve nebati yağların tamamında görülen gliseridlerin bir bileşenidir. İlk olarak zeytin yağının hidroliz ürünü olarak keşfedildi (1779).
Elde edilişi:
- Yağların sülfürik asit veya sodyum hidroksitle hidrolizi ile,
- Alkolik fermantasyonda bir yan ürün olarak,
- Sentetik olarak, tabi gazın kraking (termal parçalanma) ürünlerinden propilen başlangıç materyali alınarak,
- Allil alkolün hidrojen peroksitle WO3 katalizörlüğünde hidroksillenmesiyle elde edilir.
Özellikleri: Gliserin tatlı tada sahip, K.N. 290 derece olan renksiz bir sıvıdır. Su ve alkollerde her oranda karışır fakat eterde hemen hemen hiç çözünmez. Susuz gliserin şiddetli bir şekilde soğutulduğunda kristallenir (E.N. 18 °C). Üçlü bir alkolün göstermesi beklenilen kimyasal davranışı gösterir. Gliserinin hafif oksitlenmesi sonucu hem birincil hem de ikincil OH grupları gliseraldehit ve dihidroksiaseton teşkil edecek şekilde değiştirirler.
Kullanılışı: Gliserin yaygın bir ticari uygulama alanı bulmuştur. Ecza endüstrisinde merhem, diş macunu imalatında ve kozmetikte kullanılır. Kumaş dokumada bir amil olarak ve tütün endüstrisinde son mamülün nemini muhafaza edici olarak kullanılır. Gaz saati ve araba radyatörlerinde sulu çözelti içinde bir antifriz olarak kullanılıp bir fren sıvısı olarak bilinmektedir. Daktilo şeritlerinde higroskop olarak kullanılır. Gliserinin en önemli kullanılma alanlarından biri de patlayıcı madde endüstrisidir, nitrik asitle tepkimesinin verdiği nitrogliserin ve dinamit endüstrisinde kullanılır. Bunlara ilaveten alkid reçineleri üretiminde bir başlangıç materyalidir.
Aromatik alkoller[değiştir | kaynağı değiştir]
Aromatik alkoller yan zincirde -OH grubu bulundurduğundan aril grubu ve alifatik alkol grubu bileşiği gibi düşünülebilirler. Misal:
Benzil alkol, C6H5-CH2OH, renksiz, hoş kokulu bir sıvı olup KN. 205 °C'dir. Suda az çözünür. Elde ediliş reaksiyonu aşağıdaki gibi gösterilebilir:
- C6H5-CH2Cl+Na2CO3+H2O ® C6H5-CH2 OH+NaHCO3+NaCl
Fenil etanol, C6H5-CH2-CH2OH, gül yağının en fazla olan bileşeni olup, esterleri parfümeride çok kullanılır.
Adlandırılmaları[değiştir | kaynağı değiştir]
- Hidroksi grubunun bağlı olduğu en uzun karbon zinciri seçilir. Bu zincire karşılık gelen alkan adının sonuna -ol eki getirilir.
- Hidroksinin bağlı olduğu karbona en küçük numara gelecek şekilde karbonlar numaralandırılır.
- Hidroksi grubunun bağlı olduğu karbonun numarası alkolün adının önüne yazılır.
- Alkol bir polialkolse hidroksi sayısını gösteren ön ek, -ol ekinin önüne getirilir. (diol, triol gibi)
Elde edilişleri[değiştir | kaynağı değiştir]
Alkil halojenürlerin bazlarla tepkimesi[değiştir | kaynağı değiştir]
Alkil halojenürler, sulu sodyum hidroksitle ısıtıldıklarında nükleofilik yer değiştirme tepkimesi verir.
Aldehit ve ketonların indirgenmesi[değiştir | kaynağı değiştir]
Aldehitlerin indirgenmesiyle primer alkol, ketonların indirgenmesiyle sekonder alkol elde edilir. Tersiyer alkoller indirgenme ile elde edilemez.
Alkenlere su katılması[değiştir | kaynağı değiştir]
Asit katalizörlüğünde alkenlere su katılır. Örneğin etene su katılmasıyla etanol oluşur.
Grignard bileşiğiyle[değiştir | kaynağı değiştir]
Grignard bileşiği; formaldehitle tepkimeye girdiğinde primer alkol, diğer aldehitlerle tepkimeye girdiğinde sekonder alkol, ketonlarla tepkimeye girdiğinde tersiyer alkol oluşur.
Fiziksel özellikleri[değiştir | kaynağı değiştir]
- Alkoller yapılarında bulunan -OH hidrofil grubu sayesinde suda çözünür. Yine -OH grubu sayesinde hidrojen bağı oluşturur.
- Karbon sayısı arttıkça hidrofobik grubun baskınlığı artacağından sudaki çözünürlük azalır.
- Karbon sayısı ve -OH grubu sayısı arttıkça kaynama noktası da artar. Ancak dallanmalar arttıkça kaynama noktası düşer.
Kimyasal özellikleri[değiştir | kaynağı değiştir]
- Alkoller hidrojen halojenürlerle yer değiştirme tepkimesi verir.
- Karboksilik asitlerle kondenzasyon tepkimesi sonucu ester oluşur.
- Alkollerden ayrılma tepkimesiyle su çekilerek eter oluşur.
- Primer alkoller bir basamak yükseltgendiğinde aldehit, sekonder alkoller yükseltgendiğinde ise keton oluşur.
Kaynakça[değiştir | kaynağı değiştir]
- ^ Chemistry and Decision Making. Alcohol Chemistry and You. http://www.chemcases.com/alcohol/alc-03.htm 5 Mart 2011 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ "alkol." Güncel Türkçe Sözlük. Türk Dil Kurumu. Erişim: 2 Mart 2012
- ^ a b "alcohol." Oxford Dictionary of English 2e, Oxford University Press, 2003.


 French
French Deutsch
Deutsch