Leptospirose – Wikipédia, a enciclopédia livre
| A leptospirose, Mal de Adolf Weil ou Síndrome de Weil. | |
|---|---|
| Leptospira | |
| Especialidade | infecciologia |
| Classificação e recursos externos | |
| CID-10 | A27 |
| CID-9 | 100, 100.0, 100.9 |
| CID-11 | 751399056 |
| OMIM | 607948 |
| DiseasesDB | 7403 |
| MedlinePlus | 001376 |
| eMedicine | med/1283 emerg/856 ped/1298 |
| MeSH | D007922 |
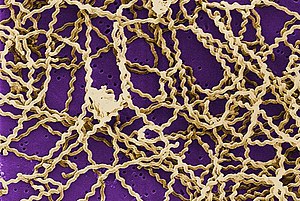
A leptospirose é uma doença infecciosa causada pela bactéria em forma de saca-rolhas chamada Leptospira. Sinais e sintomas podem variar de nenhum a leves, como dores de cabeça, dores musculares e a febres; a hemorragia severa dos pulmões ou meningite.[1] Se a infecção faz com que a pessoa fique amarela, tenha insuficiência renal e hemorragias, em seguida, ela é conhecida como doença de Weil.[2] Se ela também provoca o sangramento nos pulmões, em seguida, é conhecida como síndrome da hemorragia pulmonar grave.[2]
Até 13 tipos genéticos diferentes de Leptospira podem causar a doença em seres humanos,[3] que podem ser transmitidos tanto por animais selvagens quanto domésticos.[2] O animal mais comum a transmitir a doença são roedores.[4] Pode ser transmitida pela urina de animais ou a água ou o solo contendo urina de animais que entram em contacto com rupturas na pele, olhos, boca ou nariz.[5] Nos países em desenvolvimento, a doença ocorre mais comummente em agricultores e pessoas pobres que vivem nas cidades.[2] No mundo desenvolvido, ocorre mais comummente em pessoas envolvidas em atividades ao ar livre quentes e úmidas.[1] O diagnóstico normalmente é olhando para anticorpos contra a bactéria ou encontrando o DNA bacterial no sangue.[6]
Os esforços para prevenir a doença incluem equipamento de proteção para evitar o contato quando se trabalha com animais potencialmente infectados, lavagem após este contato, e a redução de roedores em áreas que as pessoas vivem e trabalham. O antibiótico doxiciclina, quando usado em um esforço para prevenir a infecção entre os viajantes, não tem um benefício claro. Existem vacinas para os animais para determinado tipo de Leptospira o que pode diminuir o risco de propagação para os seres humanos. Se infectado, o tratamento é com antibióticos, tais como: tetraciclina, penicilina, ou ceftriaxona.[1] A doença de Weil e a síndrome da hemorragia pulmonar grave podem resultar em taxas de mortalidade superior a 10% e 50%, respectivamente, mesmo com o tratamento.[2]
Estima-se que sete a dez milhões de pessoas são infectadas pela bactéria por ano.[7] O número de mortes por esta causa não é clara. A doença é mais comum em áreas tropicais, mas pode ocorrer em qualquer lugar.[1] Surtos podem ocorrer em favelas de países em desenvolvimento.[2] A doença foi descrita pela primeira vez pelo médico Adolf Weil, em 1886, na Alemanha.[1] Os animais que estão infectados podem não ter sintomas, sintomas leves ou graves, que podem variar para o tipo de animal.[3] Em alguns animais a Leptospira vive no trato reprodutivo, levando a transmissão durante o acasalamento.[8]
Classificação[editar | editar código-fonte]
Pode ser classificada em:
- Forma anictérica (sem amarelamento da pele): é a forma mais benigna, com poucos sintomas e auto-limitada e presente em 90% dos doentes.
- Forma ictérica (pele amarelada) ou doença de Weil: forma mais grave que acomete 10% dos doentes, podendo levar à morte.
Causas[editar | editar código-fonte]
É uma zoonose infectocontagiosa de distribuição mundial[9] causada por uma bactéria do tipo Leptospira que, eliminada principalmente na urina de roedores, permanece na água e infecta pessoas que entrem nessa água ou a consuma. Pessoas podem contaminar-se não apenas ao entrar em áreas urbanas alagadas pela chuva, como também em coleções de água doce como lagoas, represas, riachos e piscinas sem cloro. A bactéria invade por pequenas lesões de pele ou pelas mucosas em contato com a água (oral, nasal e ocular).[10]
Em caso de enchente o risco é maior já que muitas pessoas passam pela água suja com urina o que permite as bactérias infectar centenas ou milhares de pessoas na mesma hora. É mais comum em zonas rurais e em regiões quentes e úmidas de clima tropical.
Entre as principais causas, pode-se incluir a falta de saneamento básico e da rede de esgoto tratado e a falta de coleta de lixo.[9]
Fisiopatologia[editar | editar código-fonte]
A Leptospira penetra ativamente por mucosas ou lesões na pele. Após a penetração no hospedeiro, espalham-se rapidamente pela via linfática e sanguínea e os principais órgãos alvos são rins, fígado, cérebro e pulmões. Cerca de 5 a 7 dias após a infecção, aparecem os primeiros sintomas, que podem diminuir ou cessar ou podem aumentar ao desenvolver a forma mais grave da doença.[11] A síndrome da angústia respiratória aguda (SARA) é a principal causa de morte em pacientes com leptospirose grave. A liberação de componentes bacterianos como LPS e fração glicolipoprotéica causam ativação da resposta imune com agravamento do quadro clínico do paciente. O LPS da Leptospira difere das demais bactérias Gram(-) ativando TLR2 ao invés do TLR4 em humanos. A fração glicolipoprotéica (GLP) é capaz de inibir a Na+/KATPase contribuindo para o agravamento da doença, como insuficiência renal, hepatite e SARA. Além destes componentes bacterianos a bactéria apresenta moléculas de superfície celular (OMPs) como a lipoproteína LIPL32, também reconhecida pelo TLR2, encontra-se aumentada durante o curso da infecção[12] Na leptospirose também foi descrito um aumento nos ácidos graxos não esterificados (NEFA) no plasma concomitante com diminuição do nível de albumina. Esta relação: aumento dos NEFA com diminuição da albumina está diretamente relacionada à gravidade da disfunção hepática e renal.[13]
Sinais e sintomas[editar | editar código-fonte]
Como ocorre em várias outras doenças infecciosas, o quadro clínico da leptospirose varia muito de indivíduo para indivíduo. O paciente pode apresentar desde quase nenhum sintoma, o que é o mais comum, ou podem apresentar sintomas que confundem-se com de outras doenças[14] e até um quadro grave com risco de morte. O período de incubação pode variar de 2 a 45 dias. A média é 10 dias de intervalo entre a contaminação e o início dos sintomas da leptospirose que incluem[15]:
- Dor de cabeça
- Febre alta (38-40 ° C)
- Dor muscular
- Dor abdominal
- Náuseas e vômitos
- Falta de apetite
- Diarreia
- Tosse
- Calafrios
- Olhos vermelhos e inchados
- Icterícia
Sintomas incomuns incluem[15]:
- Faringite
- Conjuntivite
- Dor em ossos e articulações
- Erupções cutâneas
- Rash cutâneo sem prurido
- Gânglios, baço e/ou fígado inchados.
A maioria dos pacientes melhora em uma semana, mas algumas vezes a evolução da doença é bifásica, com alguma melhora por 10 a 15 dias seguido de nova piora dos sintomas, podendo evoluir para a fase mais grave e que possui mais complicações, conhecida como doença de Weil.[14]
Complicações[editar | editar código-fonte]
A evolução para a forma mais grave da doença ocorre em cerca de 5% a 10% de todos os casos[16] e é chamada Doença de Weil , e é caracterizada por[17]:
- Insuficiência renal aguda,
- Hemorragias,
- Icterícia (pele e olhos amarelos),
- Insuficiência hepática e insuficiência respiratória.
- Delírios.
Os pacientes que apresentam a forma mais grave da doença possuem sinais de icterícia (pele amarelada) após o terceiro dia de doença. Um sinal muito característico da forma grave é a icterícia rubínica (icterícia mais vaso dilatação, uma mistura de pele amarelada e vermelha, muitas vezes de aspecto alaranjado).
Do aparecimento dos sintomas à internação leva cerca de 5 a 6 dias, pois os casos mais leves apresentam nos primeiros dias de contágio sintomas semelhantes a outras doenças infecciosas como a dengue, a gripe e os resfriados.[18]
Diagnóstico[editar | editar código-fonte]
O diagnóstico clínico da doença não é fácil, por seus sintomas serem comuns em diversas outras infecções. O diagnóstico pode ser feito através de exames laboratoriais, sendo o bacteriológico definitivo para tal ,[19] por meio de cultivo de amostras de sangue ou urina em condições típicas, ou do teste de aglutinação microscópica, padrão-ouro pra leptospirose, mas disponível apenas em grandes laboratórios. É confirmado por meio de testes sorológicos como o Ensaio Detector de Anticorpos de Enzimas (ELISA, no acrônimo em inglês) e o PCR (sigla em inglês para Reação em Cadeia da Polimerase = Polymerase Chain Reaction). Há possibilidade de encontrar leucocitose com desvio à esquerda e plaquetopenia e enzimas musculares e exame VHS (Velocidade de Hemosendimentação) elevados. O hematócrito pode variar.
O diagnóstico do final é normalmente feito através da sorologia sanguínea.
Epidemiologia[editar | editar código-fonte]
Em países com clima tropical, a incidência média é de um caso para cada 10 mil habitantes. Em países com clima temperado/frio, a incidência média é de um caso para 100 mil habitantes. O motivo disso é que o clima quente e úmido, comum em áreas tropicais, favorece a procriação de ratos, transmissor da doença.[20]
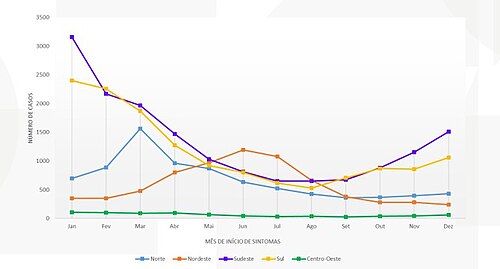
O Brasil registra uma média anual de mais de 3.600 casos e 375 óbitos da leptospirose e entre 2007 e 2017 confirmou mais de 42 mil casos. Quase metade de todos os municípios brasileiros já registraram ocorrência da doença, sendo as regiões norte e sul as mais afetadas. No país, a letalidade pode chegar a 40%.[21][22]



Em países ou municípios em que há falta de saneamento básico e rede de esgoto, a proliferação de roedores portadores da doença é favorecida, assim como em áreas onde há grande ocorrência de inundações. Pessoas que possuem profissões que tem contato direto com fluídos ou alimentos que podem ser infectados possuem mais chances de contrair a doença.[23]
Tratamento[editar | editar código-fonte]
A leptospirose é tratada com antibióticos, como a doxiciclina ou a penicilina e principalmente com estreptomicina que elimina a bactéria dos rins e, conseqüentemente, a transmissão desta doença. É importante beber apenas água tratada ou fervida para evitar reinfecções. Outros antibióticos e internação hospitalar podem ser necessários em casos graves.[24]
Leptospirose em cães[editar | editar código-fonte]
A leptospirose pode afetar os animais domésticos da mesma forma que os humanos. Também conhecida como Doença de Stuttgart ou tifo canino, acomete os cães, mas pode ser transmissível ao homem. Ao contrário dos humanos que apresentam mais o gênero Leptospira Interrogans, os cães apresentam principalmente o gênero L. canicola, mas podem apresentar também o L. icterohaemorrhagiae e o L. grippotyphosa.
A contaminação pode ocorrer através da ingestão de água e alimentos contaminados pela urina, por cheirar e lamber os órgãos genitais de outros animais contaminados e por estar em contato com animais silvestres ou de produção que apresentam a doença.
O tempo de incubação pode variar de 5 a 20 dias. Cães adultos machos e cães de centros urbanos são os que mais se infectam e a fase mais grave da doença costuma a acometer principalmente os animais mais velhos. Os animais infectados podem ser reservatório da doença por longos períodos de tempo ou pelo resto da vida e, portanto, ser fonte de doença para outras espécies.
Podem ser observados três formas da doença:
- Ícterícia: mais leve, provocada principalmente pela L. icterohaemorrhagie.
- Urêmica: provocada principalmente pela L canicola e atinge principalmente animais idosos e apresenta grande taxa de mortalidade.
- Gastrintestinal: provocada principalmente pela L. canicola.
Os sintomas podem ser febre alta, diminuição da temperatura corporal, icterícia, mudança de coloração nas mucosas conjuntivas e bucais, insuficiência renal, dor ao toque na região hepática, renal e dorsal, rigidez ao se movimentar, mudança de coloração na urina, apatia, sonolência, inapetência, vômitos, diarreias, hemorragia, erupções e úlceras na língua em casos mais avançados.
Os métodos que podem ser utilizados para dar o diagnóstico para a doença são os métodos de soro aglutinação e exames de sangue para melhor observação do agente patológico que pode ficar no sistema sanguíneo em algumas fases da doença.
É uma doença tratada por meio de antibióticos, como a penicilina. É recomendado manter o animal estável durante a fase grave da doença prevenindo grandes lesões em órgãos como o fígado e os rins. Na fase aguda, se necessário e dependendo do grau, pode-se fazer uma terapia intensiva de suporte. Além disso, quaisquer medicamentos administrados de maneira errada podem comprometer ainda mais o quadro clínico do animal.
O método de prevenção da doença é feito pelos exames preventivos e pela vacinação anual.
É indispensável à procura de um médico veterinário para avaliar o caso.[25]
Referências
- ↑ a b c d e Slack, A (julho de 2010). «Leptospirosis.». Australian Family Pphysician. 39 (7): 495–8. PMID 20628664
- ↑ a b c d e f McBride, AJ; Athanazio, DA; Reis, MG; Ko, AI (outubro de 2005). «Leptospirosis». Current Opinion in Infectious Diseases. 18 (5): 376–86. PMID 16148523. doi:10.1097/01.qco.0000178824.05715.2c
- ↑ a b «Leptospirosis» (PDF). The Center for Food Security and Public Health. Outubro de 2013. Consultado em 8 de novembro de 2014. Cópia arquivada (PDF) em 24 de novembro de 2014
- ↑ Wasiński B, Dutkiewicz J (2013). «Leptospirosis—current risk factors connected with human activity and the environment». Annals of Agricultural and Environmental Medicine. 20 (2): 239–44. PMID 23772568. Cópia arquivada em 14 de setembro de 2014
- ↑ «Leptospirosis (Infection)». Centers for Disease Control and Prevention. Consultado em 8 de novembro de 2014. Cópia arquivada em 11 de outubro de 2014
- ↑ Picardeau M (janeiro de 2013). «Diagnosis and epidemiology of leptospirosis». Médecine et Maladies Infectieuses. 43 (1): 1–9. PMID 23337900. doi:10.1016/j.medmal.2012.11.005
- ↑ «Leptospirosis». NHS. 11 de julho de 2012. Consultado em 14 de março de 2014. Cópia arquivada em 14 de março de 2014
- ↑ Faine, Solly; Adler, Ben; Bolin, Carole (1999). «Clinical Leptospirosis in Animals». Leptospira and Leptospirosis Revised 2nd ed. Melbourne, Australia: MediSci. p. 113. ISBN 0-9586326-0-X
- ↑ a b «Sorovares de Leptospira spp. Predominantes em exames sorológicos de caninos e humanos no município de Uberlândia, Estado de Minas Gerais.» (PDF)
- ↑ Perigos Ocultos nas Paisagens Brasileiras: Como evitar doenças infecciosas. Stefan Cunha Ujvari - Editora Senac, 2010
- ↑ «Leptospirose: uma doença de ocorrência além da época das chuvas!» (PDF). Arquivado do original (PDF) em 3 de outubro de 2016
- ↑ Goncalves-de-Albuquerque CF, Burth P, Silva AR, Younes-Ibrahim M, Castro-Faria-Neto HC, Castro-Faria MV. 2012. Leptospira and inflammation. Mediators Inflamm 2012:317950.
- ↑ Burth P, Younes-Ibrahim M, Santos MC, Castro-Faria Neto HC, de Castro Faria MV. 2005. Role of nonesterified unsaturated fatty acids in the pathophysiological processes of leptospiral infection. J Infect Dis 191:51-57.
- ↑ a b «Center for disease control and prevention - Singns and Symptoms»
- ↑ a b http://www.nlm.nih.gov/medlineplus/spanish/ency/article/001376.htm
- ↑ «GONCALVES, Adrelírio J. Rios; SANTINO FILHO, F.; QUAGLIOTA JR., Reynaldo and SUZUKI, Lúcia Emi. Formas graves da síndrome de Weil. Rev. Soc. Bras. Med. Trop. [online]. 1969, vol.3, n.2, p. 94-100» (PDF)
- ↑ [1]
- ↑ COSTA, Everaldo et al. Formas graves de leptospirose: aspectos clínicos, demográficos e ambientais. Revista da Sociedade Brasileira de Medicina Tropical. 34(3): 261-267, Mai-jun, 2001.
- ↑ «Leptospirose em cães: Prevalência e fatores de risco no meio rural do município de Pelotas, RS» (PDF)
- ↑ [2]
- ↑ Marteli, Alice Nardoni; Genro, Laís Vieira; Diament, Décio; Guasselli, Laurindo Antonio (setembro de 2020). «Análise espacial da leptospirose no Brasil». Saúde em Debate (126): 805–817. ISSN 2358-2898. doi:10.1590/0103-1104202012616. Consultado em 11 de setembro de 2021
- ↑ Kleber de Oliveira, Wanderson. «GUIA DE VIGILÂNCIA EM SAÚDE». Ministério da Saúde - Secretaria de Vigilância em Saúde e Coordenação-Geral de Desenvolvimento da Epidemiologia em Serviços. GUIA DE VIGILÂNCIA EM SAÚDE - Volume único (3ª edição) [2019]: 602 line feed character character in
|jornal=at position 19 (ajuda); - ↑ «Leptospirose: análise dos dados epidemiológicos de 2010 a 2014» (PDF)
- ↑ [3]
- ↑ Doenças infecciosas em animais domésticos, Joachim Beer. Editora Roca, 1988. [S.l.: s.n.] pp. 318 – 321


 French
French Deutsch
Deutsch