Koolstofmonoxide
| Koolstofmonoxide | ||||||
|---|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||||
 | ||||||
Structuurformule van koolstofmonoxide | ||||||
| Algemeen | ||||||
| Molecuulformule | CO | |||||
| IUPAC-naam | koolstofmonoxide | |||||
| Andere namen | koolstof(II)oxide, koolmonoxide, carbonyl | |||||
| Molmassa | 28,0101 g/mol | |||||
| SMILES | [O+]#[C-] | |||||
| InChI | 1/CO/c1-2 | |||||
| CAS-nummer | 630-08-0 | |||||
| EG-nummer | 211-128-3 | |||||
| PubChem | 281 | |||||
| Wikidata | Q2025 | |||||
| Beschrijving | Kleurloos en reukloos verstikkend gas | |||||
| Vergelijkbaar met | koolstofdioxide, methaan | |||||
| Waarschuwingen en veiligheidsmaatregelen | ||||||
| ||||||
| H-zinnen | H220 - H280 - H331 - H360d - H372 | |||||
| EUH-zinnen | geen | |||||
| P-zinnen | P201 - P210 - P261 - P311 - P410+P403 | |||||
| Omgang | Niet inademen, contact en blootstelling vermijden | |||||
| Opslag | Indien bewaard in gasfles, temperatuur niet boven 50 °C laten uitkomen; stevig gesloten houden verwijderd van direct zonlicht, hitte, vonken en open vlammen vanwege ontvlambaarheid | |||||
| EG-Index-nummer | 006-001-00-2 | |||||
| VN-nummer | 1016 | |||||
| MAC-waarde | 29 mg/m³ | |||||
| Fysische eigenschappen | ||||||
| Aggregatietoestand | gasvormig | |||||
| Kleur | kleurloos | |||||
| Dichtheid | (bij 0°C) 0,00125 g/cm³ | |||||
| Smeltpunt | −205,06 °C | |||||
| Kookpunt | −191,47 °C | |||||
| Goed oplosbaar in | methanol, ethanol | |||||
| Thermodynamische eigenschappen | ||||||
| ΔfH | −110,5 kJ/mol | |||||
| S | 197,7 J/mol·K | |||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||||
| ||||||
Koolstofmonoxide, koolstofmono-oxide of koolmonoxide, vroeger ook wel kolendamp genoemd, is een polaire anorganische verbinding van koolstof en zuurstof, met als brutoformule CO. In de volksmond wordt het vaak gewoonweg CO genoemd. Het is een kleurloos gas dat onder meer ontstaat door onvolledige verbranding van koolstof, fossiele brandstoffen of andere brandbare koolstofverbindingen (de meeste organische verbindingen). Het is een vrij belangrijke stof in de chemische industrie. Koolstofmonoxide is giftig, kleurloos en reukloos. Hierdoor is het erg gevaarlijk. Het gas is fractioneel lichter dan lucht.
Voorkomen[bewerken | brontekst bewerken]
Koolstofmonoxide is een van de schadelijke stoffen in de uitlaatgassen van auto's en tabaksrook[1] (rokers hebben een meetbaar percentage koolstofmonoxide in hun bloed). Omdat koolstof vroeger in de vorm van steenkool een belangrijke brandstof was voor het verwarmen van huizen, waarbij weleens ongelukken voorkwamen bij slecht onderhouden schoorstenen en kachels, staat koolstofmonoxide ook wel bekend als kolendamp. Berucht is het ontstaan van koolstofmonoxide bij verbranding van aardgas in kachels en geisers in slecht geventileerde ruimtes. Daarbij kan koolstofmonoxidevergiftiging optreden.
Koolstofmonoxide komt van nature in het milieu voor ten gevolge van vulkaanuitbarstingen (samen met onder andere zwaveldioxide, koolstofdioxide, waterstofsulfide en koolstofdisulfide), ontgassing van moerassen (samen met methaan) en bosbranden. Ook bij tal van industriële activiteiten (olieraffinaderijen en verbrandingsovens) komt het gas vrij.
Synthese[bewerken | brontekst bewerken]
Koolstofmonoxide ontstaat onder andere bij onvolledige verbranding van koolstof:
De verbinding kan echter ook gevormd worden bij ontleding van andere verbindingen bij verhitting, bijvoorbeeld van oxalaten:
Op kleine schaal (laboratoriumschaal) kan het ook gesynthetiseerd worden uitgaande van een aantal specifieke precursoren:
- Reactie tussen chloroform en cesiumhydroxide
- Reactie tussen triethylamine, mierenzuur en methaansulfonylchloride
- Reactie tussen methyldifenylsilacarbonzuur en kaliumfluoride
- Reactie tussen tetrafenyldimethyldisilaan en cesiumfluoride
Structuur en eigenschappen[bewerken | brontekst bewerken]
De structuur van de molecule is per definitie lineair (koolstofmonoxide is immers diatomisch) en wordt het beste beschreven met behulp van de molecuulorbitaaltheorie. De lengte van de binding (111 pm) duidt erop dat er partieel drievoudige bindingskarakter aanwezig is. Koolstofmonoxide bezit een klein dipoolmoment.
Klassieke chemische beschrijving[bewerken | brontekst bewerken]
In de geschiedenis van de beschrijving van de chemische binding heeft koolstofmonoxide vaak voor problemen gezorgd. In de Lewistheorie ging men uit van het idee dat er een neiging bestond een octet te willen vormen en dat bindingen voortkwamen uit de noodzaak elektronenparen te delen tussen atomen om aan deze octetregel te voldoen. In koolstofmonoxide zijn in totaal 10 valentie-elektronen aanwezig (4 van koolstof en 6 van zuurstof). Het aantal gewenste elektronen (om 2 octetten te vormen) bedraagt echter 16, dus er zullen formele ladingen optreden in de molecule. In 1919 stelde Irving Langmuir een structuurformule voor met een drievoudige binding tussen koolstof en zuurstof. Ieder element draagt daarbij 1 vrij elektronenpaar:
Het probleem met deze structuur is dat de formele lading van koolstof hier −1 en van zuurstof +1 bedraagt. Deze formele ladingen zijn echter het omgekeerde van wat men op grond van de elektronegativiteit zou verwachten: koolstof is elektropositiever dan zuurstof en verdraagt gemakkelijker een positieve dan een negatieve lading. Het omgekeerde geldt voor zuurstof.
Dit bracht Linus Pauling ertoe de moleculen weer te geven met 3 resonantiestructuren:
De eerste structuur is de door Langmuir voorgestelde. De middelste structuur bezit geen formele ladingen en ziet er dus een stuk aannemelijker uit, maar het koolstofatoom heeft geen octet meer. Bovendien is de gemeten bindingsafstand in koolstofmonoxide korter dan wat voor een dubbele binding verwacht kan worden. Voor de derde structuur is de formele lading in overeenstemming met de elektronegativiteit van ieder atoom, maar het koolstofatoom heeft nog slechts vier elektronen rond zich en is dus absoluut niet stabiel.
Kwantumchemische beschrijving[bewerken | brontekst bewerken]
Het feit dat geen van de drie voorgestelde resonantiestructuren voldoet aan de klassieke chemische beschrijving van de binding, bewijst de fundamentele tekortkomingen ervan. De kwantummechanica en theoretische chemie brachten daarin verandering. Een beschrijving met moleculaire orbitalen laat zien dat er drie bindingen en partiële ladingen aanwezig zijn. Beide conclusies zijn in overeenstemming met experimenteel vastgestelde waarden wat betreft de bindingslengte en de elektronegativiteit.
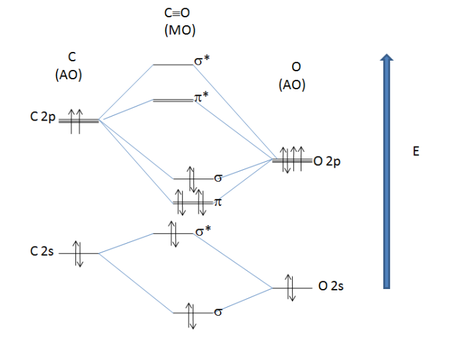
In de kwantumchemische beschrijving zijn er elektronenparen in orbitalen die zich over de gehele molecule uitstrekken: ze zijn dus niet gelokaliseerd op 1 atoom. Twee elektronen bevinden zich elk in het bindende σ- en antibindende σ*-orbitaal. Zij zijn opgebouwd uit de 2s-orbitalen (atomaire orbitalen) van de beide atomen. Gezamenlijk dragen zij niet tot binding bij omdat de bindende eigenschappen van het σ-moleculair orbitaal opgeheven worden door die van het antibindende. Er worden echter drie elektronenparen in de σ- en π-orbitalen gevormd door de orbitaaloverlap van 2p-orbitalen van beide atomen. De antibindende σ*- en π*-moleculaire orbitalen zijn niet bezet: dit geeft aanleiding tot een drievoudige binding. Door opmenging van de σ(2s)- en σ(2p)-orbitalen komt het σ(2p)-orbitaal iets hoger te liggen dan het π(2p)-orbitaal. De HOMO (het hoogst bezette moleculaire orbitaal) is dus het σ(2p)-orbitaal en het laagste onbezette (de LUMO) is het π*(2p)-orbitaal.
De gevulde σ(2p)- en π(2p)-orbitalen bezitten ten gevolge van het elektronegativiteitsverschil van de atomen iets meer of minder zuurstof- dan wel koolstofkarakter. Dit geeft zuurstof een partiële negatieve lading (δ−) en koolstof een partieel positieve (δ+). Het eindresultaat is dus wellicht het best samen te vatten als volgende structuur:
De negatieve lading ligt hierbij dus, in tegenstelling tot wat bij de Lewis-structuur het geval was, op het meest elektronegatieve atoom.
Coördinatiechemie[bewerken | brontekst bewerken]
Koolstofmonoxide kan sterke interacties aangaan met een groot aantal metalen en metaalionen, vooral van de overgangsmetalen. De resulterende verbindingen worden carbonylcomplexen genoemd. De symmetrie (de vorm) van de HOMO en de LUMO zijn daar grotendeels verantwoordelijk voor. Het gevulde σ(2p)-orbitaal (de HOMO) bezit een grote coëfficiënt (een grote atomaire bijdrage) aan de kant van het koolstofatoom en kan elektronendichtheid doneren aan een metaalatoom, bijvoorbeeld door een σ-binding aan te gaan met de dx2-y2-orbitalen. Het lege π*(2p)-orbitaal (de LUMO) kan via een π-interactie elektronendichtheid van het metaalion terug accepteren, op voorwaarde dat deze gevulde orbitalen van geschikte symmetrie (zoals het dxz-orbitaal) bezit. Deze vorm van wederzijdse wisselwerking wordt ook wel pi-backbonding (terugbinding via het π-moleculaire orbitaal) genoemd. Koolstofmonoxide is aldus een pi-acceptorligand en vormt gemakkelijk low-spin-complexen (het genereert een sterk ligandveld). De pi-backbonding verklaart de stabiliteit van een aantal carbonylcomplexen zoals chroomhexacarbonyl, molybdeenhexacarbonyl, wolfraamhexacarbonyl, ijzerpentacarbonyl en nikkeltetracarbonyl. Deze laatste verbinding wordt zelfs gevormd wanneer nikkel gewoon wordt blootgesteld aan koolstofmonoxide.
Reacties met niet-metalen[bewerken | brontekst bewerken]
Het oxidatiegetal van koolstof in koolstofmonoxide is +II, in plaats van het gebruikelijke +IV. Het kan daarom verder geoxideerd worden tot koolstofdioxide en is daarom brandbaar:
Koolstofmonoxide kan onder invloed van licht directe reacties ondergaan met de halogenen. Met chloorgas wordt bijvoorbeeld fosgeen gevormd:
Zwavel reageert bij hogere temperaturen tot carbonylsulfide:
Toxicologie en veiligheid[bewerken | brontekst bewerken]
Koolstofmonoxide is een giftig gas. In het bloed hecht het zich aan het zuurstoftransport-eiwit hemoglobine in rode bloedcellen, waarbij het zuurstofgas (O2) verdringt. Dit is te wijten aan de sterke coördinatiebinding (pi-backbonding) met het ijzer in hemoglobine. Het vermogen van koolstofmonoxide om zich vast te hechten op dit eiwit is circa 240 keer zo groot als dat van zuurstof. Dat betekent dat zelfs bij een geringe concentratie van koolstofmonoxide in de lucht relatief veel koolstofmonoxide in het bloed terecht kan komen en er vergiftigingsverschijnselen kunnen optreden. De symptomen van koolstofmonoxidevergiftiging zijn hoofdpijn, misselijkheid, duizeligheid en vermoeidheid. Bij langere blootstelling wordt dit gevolgd door bewusteloosheid en ten slotte de dood door zuurstofgebrek in de hersenen.
Tijdens de Tweede Wereldoorlog werd koolstofmonoxide onder andere gebruikt in de gaskamers van de vernietigingskampen Majdanek, Sobibór, Bełżec en Treblinka. Ook maakte men gebruik van zogenaamde gaswagens. Dit waren gesloten vrachtwagens die gevangenen konden vervoeren (ze gingen zogenaamd op transport). De chauffeur kon via een eenvoudig mechanisme de uitlaatgassen (die koolstofmonoxide bevatten) de laadruimte inleiden, terwijl de wagen naar een massabegraafplaats of crematorium reed.
Soms wordt zelfmoord gepleegd door het inademen van de koolstofmonoxide bevattende uitlaatgassen van verbrandingsmotoren.
Stadsgas[bewerken | brontekst bewerken]
Voordat in de jaren 60 van de 20e eeuw aardgas in gebruik werd genomen, werd stadsgas gebruikt (ook wel kolengas genoemd), een gas dat hoofdzakelijk uit koolstofmonoxide, methaan en waterstof bestond. Dit gas werd vooral gebruikt voor verlichting en om op te koken. Het werd uit steenkool gemaakt in gasfabrieken. Het stadsgas was beschikbaar in iedere woning en werd soms gebruikt om zelfmoord te plegen. De persoon ging dan met het hoofd in de oven liggen en raakte snel buiten bewustzijn. Ter voorkoming van accidentele vergiftiging en vanwege explosiegevaar werd aan het stadsgas een sterke kunstmatige gaslucht (een thiol) toegevoegd opdat gaslekken snel zouden opvallen.
Zie ook[bewerken | brontekst bewerken]
Externe link[bewerken | brontekst bewerken]
Bronnen, noten en/of referenties
|
- ↑ 9 schadelijke stoffen in tabaksrook (WHO). RIVM. Geraadpleegd op 5 maart 2024.


 French
French Deutsch
Deutsch










