Dimethylformamide
| Dimethylformamide | |||||
|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | |||||
 | |||||
Structuurformule van dimethylformamide | |||||
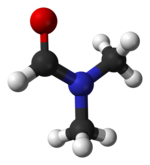 | |||||
Molecuulmodel van dimethylformamide | |||||
| Algemeen | |||||
| Molecuulformule | C3H7NO | ||||
| IUPAC-naam | N,N-dimethylformamide | ||||
| Andere namen | N,N-dimethylmethaanamide, DMF, DMFA | ||||
| Molmassa | 73,09378 g/mol | ||||
| SMILES | CN(C)C=O | ||||
| InChI | 1S/C3H7NO/c1-4(2)3-5/h3H,1-2H3 | ||||
| CAS-nummer | 68-12-2 | ||||
| EG-nummer | 200-679-5 | ||||
| PubChem | 6228 | ||||
| Wikidata | Q409298 | ||||
| Beschrijving | Kleurloze, in zuivere toestand geurloze vloeistof | ||||
| Vergelijkbaar met | dimethylaceetamide formamide N-methylformamide | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H226 - H319 - H312 - H332 - H360d[1] | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P201 - P280 - P305+P351+P338 - P308+P313[1] | ||||
| EG-Index-nummer | 616-001-00-X | ||||
| VN-nummer | 2265 | ||||
| ADR-klasse | Gevarenklasse 3 | ||||
| Fysische eigenschappen | |||||
| Aggregatietoestand | vloeibaar | ||||
| Kleur | kleurloos | ||||
| Dichtheid | 0,95[2] g/cm³ | ||||
| Smeltpunt | −61[2] °C | ||||
| Kookpunt | 153[2] °C | ||||
| Vlampunt | 58[2] °C | ||||
| Zelfontbrandings- temperatuur | 440[2] °C | ||||
| Oplosbaarheid in water | mengbaar g/L | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Dimethylformamide of DMF (IUPAC-naam: N,N-dimethylformamide) is een kleurloze vloeistof, mengbaar met water en een groot aantal organische oplosmiddelen. Zuivere DMF is geurloos terwijl gedegradeerde DMF vaak een vislucht heeft vanwege onzuiverheden van dimethylamine. Het is een veelgebruikt oplosmiddel in chemische reacties.
De naam is afgeleid van het feit dat het een formamide (het amide van mierenzuur) is met twee methylgroepen, beide op het stikstofatoom.
Synthese[bewerken | brontekst bewerken]
Dimethylformamide wordt gesynthetiseerd door middel van de reactie van mierenzuur met dimethylamine, of van de gekatalyseerde reactie van dimethylamine en koolstofmonoxide bij lage druk en temperatuur.
Eigenschappen en reacties[bewerken | brontekst bewerken]
Dimethylformamide is een polair aprotisch oplosmiddel met een hoog kookpunt. Het is niet stabiel in de aanwezigheid van sterke basen, zoals natronloog, of sterke zuren als zoutzuur of zwavelzuur. Het wordt dan gehydrolyseerd naar mierenzuur en dimethylamine, vooral bij hogere temperaturen.
Toepassingen[bewerken | brontekst bewerken]
Dimethylformamide wordt voornamelijk gebruikt als een oplosmiddel dat weinig verdampt. DMF wordt gebruikt in de productie van acrylvezels en plastics. Andere toepassingen zijn onder meer als oplosmiddel voor peptidekoppeling in geneesmiddelen, de productie van pesticiden en de productie van synthetisch leer.[3] DMF wordt als reagens gebruikt in de Bouveault-aldehydesynthese en in de Vilsmeier-Haack-reactie, die methoden zijn om aldehydes te vormen.
Het proton-NMR-spectrum van dimethylformamide heeft twee singlets voor de methylgroepen omdat de rotatietijd om de koolstof-stikstof-binding langzamer is dan de NMR-tijdsschaal.
Dimethylformamide dringt binnen in de meeste plastics en laat deze opzwellen. Het wordt daarom regelmatig gebruikt in verfstripper.
Toxicologie en veiligheid[bewerken | brontekst bewerken]
Reacties met natriumhydride in dimethylformamide als oplosmiddel zijn enigszins gevaarlijk. Exotherme degradatie is waargenomen bij temperaturen van slechts 26 °C.[4][5] In een laboratorium wordt deze warmte eenvoudig opgevangen met een koelbad, maar op fabrieksschaal kan dit ongelukken veroorzaken.
Enkele bronnen tonen aan dat dimethylformamide leverschade,[6] kanker[7] en aangeboren afwijkingen[8] zou kunnen veroorzaken. Op sommige plaatsen wordt het vrouwen preventief verboden te werken met dimethylformamide. Voor veel reacties kan DMF vervangen worden door dimethylsulfoxide (DMSO).
Externe links[bewerken | brontekst bewerken]
Bronnen, noten en/of referenties
|


 French
French Deutsch
Deutsch

