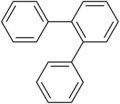
Terfenile
| p-terfenile | |
|---|---|
 | |
| Nome IUPAC | |
| 1,4-difenilbenzene | |
| Nomi alternativi | |
| p-difenilbenzene | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C18H14 |
| Aspetto | polvere bianca[1] |
| Numero CAS | Numero CAS per l'isomero para; altri numeri CAS associati sono: 92-06-8 (meta) 84-15-1 (ortho) 26140-60-3 (non specificato) |
| Numero EINECS | 247-477-3 |
| PubChem | 7115 |
| SMILES | C1=CC=C(C=C1)C2=CC=C(C=C2)C3=CC=CC=C3 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,234[2] |
| Densità (kg·m−3, in c.s.) | 7,95[2] |
| Solubilità in acqua | insolubile[1] |
| Temperatura di fusione | 212-214 °C[1] 212-213 °C[3] |
| Temperatura di ebollizione | 389 °C[3] |
| Indicazioni di sicurezza | |
| Punto di fiamma | 207 °C[3] |
| Simboli di rischio chimico | |
  | |
| Frasi H | 315 - 319 - 335 - 400 |
| Consigli P | 261 - 273 - 305+351+338 |
I terfenili sono un gruppo di idrocarburi aromatici costituiti da una catena di tre anelli benzenici. Sono noti anche con il nome di difenilbenzeni o trifenili. Sono possibili tre isomeri, noti come p-, o-, m-terfenile, in base alla posizione del terzo gruppo fenile rispetto all'anello benzenico centrale.
Derivati dei terfenili sono stati scoperti per la prima volta nella seconda metà del XIX secolo sotto forma di pigmenti contenuti all'interno di alcune specie di funghi. La prima delucidazione della struttura chimica di sostanze aventi lo scheletro di atomi di carbonio riconducibile ai terfenili è stata compiuta ad opera di Kögl, che descrisse in particolare due composti: l'acido poliporico e l'atromentina.
I derivati chimici dei terfenili spesso presentano una ossidazione chinonica del benzene centrale per cui è facile che vengano classificati come fenilchinoni.
Formule di struttura dei tre isomeri[modifica | modifica wikitesto]
- ortho-terfenile
- meta-terfenile
- para-terfenile
Terfenili naturali[modifica | modifica wikitesto]
Dei terfenili sono presenti in natura specialmente i derivati del p-terfenile, meno frequenti sono i derivati del m-terfenile, mentre sono tuttora sconosciuti i derivati dell'o-terfenile. Nello specifico, i p-terfenili, diffusissimi nel regno dei funghi, non sono ancora stati trovati nel regno vegetale; viceversa non esiste segnalazione di m-terfenili nel regno dei funghi.
Utilizzi industriali[modifica | modifica wikitesto]
Il p-terfenile è l'isomero più comune; esso è utilizzato come colorante per laser a coloranti e ingrediente per filtri solari[1].
I terfenili commercialmente disponibili sono solitamente una miscela dei tre isomeri. Questa miscela è utilizzata nella produzione di terfenili policlorurati, che in passato erano impiegati come agenti di accumulo e trasferimento termico[1].
Attività farmacologica[modifica | modifica wikitesto]
Alcuni terfenili sono spesso presenti nei funghi di normale consumo alimentare, ma per alcuni di essi è stata verificata una significativa attività farmacologica come immunosoppressori, neuroprotettori, antitrombinici, anticoagulanti, inibitori enzimatici specifici, agenti citotossici.
Farmaci ottenuti impiegando i terfenili naturali dotati di attività o derivati specifici hanno suscitato notevole interesse in virtù del fatto che la sintesi chimica di questi prodotti è relativamente semplice, non essendovi centri chirali.
Note[modifica | modifica wikitesto]
- ^ a b c d e p-Terphenyl su chemicalland21.com
- ^ a b Scheda di sicurezza del p-terfenile - ScienceLab
- ^ a b c p-Terphenyl sul sito web di Sigma-Aldrich
Bibliografia[modifica | modifica wikitesto]
- Ji-Kai Liu, Natural Terphenyls: Developments since 1877, Chem. Rev. 2006, 106, 2209-2223
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Terfenile
Wikimedia Commons contiene immagini o altri file su Terfenile
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) p-Terphenyl - Oregon Laser Medical Center


 French
French Deutsch
Deutsch