Legame a idrogeno
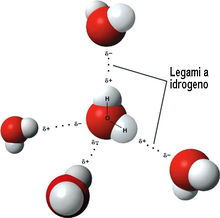
Il legame a idrogeno o ponte a idrogeno è un caso particolare di forza intermolecolare (ma nei casi opportuni anche intramolecolare) in cui è implicato un atomo di idrogeno coinvolto in un legame covalente con elementi molto elettronegativi (come fluoro (), ossigeno (), azoto ()),[1] i quali attraggono a sé gli elettroni di valenza, acquisendo una parziale carica negativa lasciando l'idrogeno con una parziale carica positiva .[2] Contemporaneamente l'idrogeno viene attratto da un atomo elettronegativo (che deve presentare un doppietto elettronico non condiviso) di una molecola vicina.
Descrizione[modifica | modifica wikitesto]
Il legame a idrogeno è l'attrazione elettrostatica tra un atomo di idrogeno recante una parziale carica elettrica positiva e un doppietto elettronico solitario di un elemento fortemente elettronegativo (fluoro, ossigeno o azoto).
Ad esempio nel radicale idrossile e nell'anione idrossido è presente una parziale carica negativa sull'ossigeno e una equivalente carica positiva sull'idrogeno, quindi tali composti si polarizzano parzialmente (dipolo permanente).
Se questo gruppo ne incontra un altro polare (ad esempio un gruppo carbonile), si crea una interazione elettrostatica.
La forza del legame idrogeno è variabile a seconda dei casi (comunque solitamente compresa fra 10-60 kJ/mol). Il legame idrogeno è forte se l'elemento elettronegativo è l'ossigeno, l'azoto o il fluoro, mentre è debole o assente per elementi della tavola periodica a periodi successivi al secondo. A temperatura ambiente nell'acqua pura, dipende dalla permittività elettrica del mezzo; infatti, essendo un legame elettrostatico per esso vale la legge di Coulomb. Comunque è nettamente più debole del legame ionico e del legame covalente, ma è nettamente più forte delle forze di van der Waals ed è il tipo più forte di interazione intermolecolare (escluse le forze ione-dipolo).

Un'importante osservazione è che esso è un legame su base elettrostatica ma altamente direzionale: ad esempio nell'acqua l'atomo di ossigeno, l'idrogeno, il doppietto elettronico e l'altro ossigeno di un'altra molecola d'acqua debbono essere allineati lungo lo stesso asse (quindi costituenti un angolo piatto, 180°) per avere un legame massimamente forte, altrimenti daranno luogo a un legame di forza inferiore. Ciò può risultare di cruciale importanza nel DNA, in cui vi sono moltissimi legami idrogeno tra gli acidi nucleici, o nel ripiegamento di proteine dove la diversa intensità di queste interazioni dà forma a una precisa conformazione della proteina, quella in grado di renderla funzionale.

Il legame idrogeno è presente nell'acqua sia allo stato liquido che allo stato solido, ed è responsabile della sua relativamente alta temperatura di ebollizione (se paragonata per esempio all'acido solfidrico (), che pur avendo peso molecolare maggiore è significativamente meno polare). In particolare, senza il contributo dei legami idrogeno, l'acqua bollirebbe a .
Una caratteristica peculiare del legame idrogeno è quella di mantenere le molecole interessate più distanti fra loro rispetto agli altri tipi di legami. Altra caratteristica è il comportamento del legame idrogeno nell'acqua: allo stato solido una molecola d'acqua è legata con legame idrogeno ad altre quattro molecole, allo stato liquido questa struttura viene demolita e le molecole non sono più costrette in una struttura espansa come quella del solido, è per questo che il ghiaccio è meno denso dell'acqua, la temperatura infatti induce la rottura di alcuni legami idrogeno presenti nel ghiaccio e ciò permette alle molecole di compattarsi (aumento di densità da solido a liquido fino a , poi calo).
Il legame idrogeno è presente nelle proteine (principalmente nelle strutture secondarie: alfa elica e beta foglietto) e negli acidi nucleici è una delle forze che tiene uniti i due filamenti del DNA.
Note[modifica | modifica wikitesto]
- ^ (EN) IUPAC Gold Book, "hydrogen bond"
- ^ Rolla, p. 87.
Bibliografia[modifica | modifica wikitesto]
- Luigi Rolla, Chimica e mineralogia. Per le Scuole superiori, 29ª ed., Dante Alighieri, 1987.
Voci correlate[modifica | modifica wikitesto]
- Acqua
- Forza di van der Waals
- Dipolo molecolare
- Legame chimico
- Elettronegatività
- Dimero dell'acqua
- Legame ad alogeno
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su legame a idrogeno
Wikimedia Commons contiene immagini o altri file su legame a idrogeno
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) hydrogen bonding, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | LCCN (EN) sh85063424 · GND (DE) 4064787-0 · BNF (FR) cb12260675k (data) · J9U (EN, HE) 987007533740205171 · NDL (EN, JA) 00571632 |
|---|


 French
French Deutsch
Deutsch








