Anomeria
In chimica, l'anomeria consiste in una isomeria geometrica peculiare dei carboidrati all'interno della categoria degli epimeri.
L'anomeria si realizza quando uno dei due stereoisomeri di un saccaride ciclico differisce solamente nella configurazione del carbonio emiacetalico o di quello emichetalico, che diviene quindi il carbonio anomerico.
Il processo di conversione di un anomero nell'altro viene detto "anomerizzazione" ed è l'analogo anomerico dell'epimerizzazione tra gli epimeri.
Nomenclatura[modifica | modifica wikitesto]
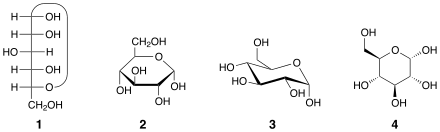
1 = Proiezione di Fischer
2 = Proiezione di Haworth
3 = Rappresentazione conformazionale
4 = Configurazione assoluta
Due anomeri sono designati alfa (α) o beta (β), in funzione della relazione configurazionale tra il centro anomerico e l'atomo anomerico di riferimento; essi sono pertanto degli stereodescrittori relativi.[1]
Il centro anomerico negli emiacetali è il carbonio anomerico C-1, che è attaccato all'ossigeno emiacetalico nell'anello; negli emichetali è il carbonio C-2, attaccato all'ossigeno emichetalico. Negli aldoesosi e nei carboidrati a più basso numero di carbonio, l'atomo anomerico di riferimento è lo stereocentro più lontano dall'atomo anomerico nell'anello . Nell'α-D-glucopiranosio l'atomo di riferimento è il C-6.
Se nella proiezione di Fischer[2] l'atomo di ossigeno esociclico nel centro anomerico è in isomeria cis (cioè dallo stesso lato) con l'ossigeno esociclico attaccato all'atomo di riferimento anomerico (nel gruppo OH), allora l'anomero è designato α. Se i due atomi di ossigeno sono in isomeria trans (su lati opposti), l'anomero è definito β.[3] Per i composti ciclici tuttavia l'uso della proiezione di Fischer è complicato e poco comune.
Se si confrontano le configurazioni assolute del carbonio anomerico e dell'atomo di riferimento, allora esse sono diverse (S,R o R,S) nell'anomero α e uguali (R,R or S,S) nell'anomero β.
Esempi[modifica | modifica wikitesto]
Quando uno zucchero forma una soluzione acquosa esso tende ad assumere una struttura emiacetalica o emichetalica più stabile. In questo modo formando un ciclo a sei atomi, definito ciclo piranosico per la similitudine con la struttura del pirano, l'idrossile del carbonio 5 si lega con il carbonio carbonilico in posizione 1: tale atomo di carbonio, definito carbonio anomerico, diviene un nuovo stereocentro. Il gruppo -OH formatosi sul carbonio anomerico può trovarsi in due differenti posizioni alternative: sotto il piano in cui giace la molecola ciclica oppure sopra tale piano. I due differenti isomeri vengono in questo caso definiti anomeri.[4] In particolare l'anomero α rappresenta la struttura in cui l'ossidrile sul carbonio 1 si trova sotto al piano della molecola, mentre nell'anomero β questo ossidrile è sito sopra il piano della molecola.
Analoga discussione è valida per l'altra forma ciclica stabile in cui possono presentarsi i carboidrati, ovvero la struttura furanosica (per analogia con il furano) con ciclo penta-atomico formato quando stavolta il gruppo -OH del carbonio 4 si lega al carbonile in posizione 1.
In generale l'anomero β risulta la forma più stabile in quanto la repulsione tra -OH (1) e l'ossidrile adiacente è minore, essendo il gruppo ossidrilico sul carbonio anomerico in posizione equatoriale (repulsioni diassiali minime). Esistono però delle eccezioni, come le soluzioni acquose di mannosio, in cui prevale l'anomero α (effetto anomerico).
Anomerizzazione[modifica | modifica wikitesto]
L'anomerizzazione è il processo di conversione di un anomero nell'altro. Per gli zuccheri riducenti, l'anomerizzazione avviene rapidamente in soluzione; il processo è reversibile e tipicamente tende a produrre una mistura anomerica in cui si raggiunge una configurazione di equilibrio tra i due singoli anomeri.
Il rapporto tra i due anomeri è specifico per un determinato zucchero. Nel caso del D-glucosio, indipendentemente dalla configurazione iniziale, la soluzione tenderà ad una mistura con all'incirca il 64% di β-D-glucopiranosio e il 36% di α-D-glucopiranosio. Al variare del rapporto relativo dei due anomeri, varia anche la rotazione ottica; questo fenomeno è noto come mutarotazione.
Proprietà fisiche e stabilità[modifica | modifica wikitesto]
La diversità nella struttura degli anomeri comporta anche differenti effetti stabilizzanti e destabilizzanti. I maggiori contributi alla stabilità di un dato anomero sono dati da:
- Effetto anomerico, che stabilizza l'anomero che possiede un gruppo elettronegativo (tipicamente ossigeno o azoto) in orientamento assiale sull'anello. L'effetto viene annullato in solventi polari come l'acqua.
- Interazione 1,3-diassiale (struttura a sedia), che solitamente destabilizza l'anomero che ha il gruppo anomerico in orientamento assiale sull'anello. Questo effetto è particolarmente evidente nei piranosi e in altri composti ciclici a sei atomi. L'effetto diventa importante in acqua.
- Legame a idrogeno tra il gruppo anomerico e altri gruppi dell'anello, che portano ad una stabilizzazione dell'anomero.
- Repulsione dipolare tra il gruppo anomerico e altri gruppi dell'anello, che portano alla destabilizzazione dell'anomero.
Nel caso del D-glucopiranoside, l'anomero β è il più stabile. L'effetto principale in questo caso è l'assenza di interazioni 1,3-diassiali. Per il D-mannopiranosio è l'anomero α il più stabile, perché questa forma evita la repulsione dipolare tra l'ossidrile anomerico e l'ossidrile sul carbonio adiacente nell'anello.
Poiché i due anomeri sono l'uno il diastereoisomero dell'altro, essi possono anche differire nelle proprietà chimiche e fisiche. Una delle più importanti proprietà fisiche che sono utilizzate per studiare gli anomeri è il potere rotatorio, che può essere valutato attraverso la polarimetria.
Note[modifica | modifica wikitesto]
- ^ IUPAC Gold Book α (alpha), β (beta) Archiviato il 22 novembre 2016 in Internet Archive.
- ^ Nomenclatura dei Carboidrati 2-Carb-5
- ^ Nomenclature of Carbohydrates (Recommendations 1996) PDF
- ^ (EN) anomers, IUPAC Gold Book
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Anomeria
Wikimedia Commons contiene immagini o altri file su Anomeria


 French
French Deutsch
Deutsch
