Traitement et gestion de la Covid-19 — Wikipédia
En septembre 2021, on ne connaissait pas de traitement spécifique ou de cure efficace à la maladie à coronavirus 2019 (Covid-19), causée par le virus SARS-CoV-2[1],[2]. Ainsi, la pierre angulaire de la gestion de la Covid-19 consistait en des soins de soutien, qui comprenaient le soulagement des symptômes, l'hydratation, l'oxygénothérapie au besoin, et des médicaments ou des dispositifs pour soutenir d'autres organes vitaux affectés[3],[4],[5],[6]. Les anticorps monoclonaux ont aussi montré une certaine efficacité dans le traitement de cette maladie, tant en curatif qu’en préventif.
Gestion générale[modifier | modifier le code]
La plupart des cas de Covid-19 étaient légers. Dans ces cas, les soins de soutien comprenaient des médicaments tels que le paracétamol ou les AINS pour soulager les symptômes (fièvre, douleurs musculaires, toux), un apport adéquat en liquides et le repos[7],[2],[8],[9]. Une bonne hygiène personnelle et une alimentation saine étaient également recommandées[10]. Le CDC américain recommandait à ceux qui soupçonnent être porteurs du virus de s'isoler à la maison et de porter un masque facial[11].
Les personnes atteintes plus sévèrement peuvent nécessiter une hospitalisation. Chez les personnes ayant de faibles niveaux d'oxygène, l'utilisation de la dexaméthasone en combinaison avec un inhibiteur de l'interleukine-6 (Tocilizumab ou Sarilumab) était fortement recommandée par l'OMS, car elle peut réduire le risque de décès[12],[13],[14],[15]. Une ventilation non invasive et, finalement, une admission dans une unité de soins intensifs pour une ventilation mécanique peuvent être nécessaires pour soutenir la respiration[16]. Les avantages de l'oxygénation par membrane extracorporelle (ECMO) a été étudiée pour traiter l'insuffisance respiratoire[17],[18].
Plusieurs traitements expérimentaux étaient activement étudiés dans le cadre d'essais cliniques[1]. D'autres ont été jugés prometteurs au début de la pandémie, comme l'hydroxychloroquine et le lopinavir/ritonavir, mais des recherches ultérieures ont révélé qu'ils étaient inefficaces, voire nocifs. Malgré les recherches, il n'y a toujours pas suffisamment de preuves de haute qualité pour recommander un traitement dit précoce[19],. Néanmoins, aux États-Unis, une thérapie à base d'anticorps monoclonaux est disponible pour une utilisation précoce dans les cas à risque élevé d'évolution vers une maladie grave[20],[21]. L'antiviral remdesivir est disponible aux États-Unis, au Canada, en Australie et dans plusieurs autres pays avec des restrictions variables ; cependant, il n'est pas recommandé pour les personnes ayant besoin d'une ventilation mécanique. Son utilisation est découragée par l'Organisation mondiale de la santé (OMS) en raison des preuves limitées de son efficacité[22].
Certaines personnes peuvent éprouver des symptômes persistants ou des séquelles après la guérison de l'infection ; ceci est connu sous le nom de Covid long . Les informations sur la meilleure prise en charge et la meilleure réadaptation pour cette condition sont encore limitées[16].
L'OMS, la Commission nationale chinoise de la santé, le National Institute for Health and Care Excellence du Royaume-Uni et les National Institutes of Health des États-Unis, parmi d'autres organismes et agences du monde entier, ont tous publié des recommandations et des lignes directrices pour traiter des personnes atteintes de Covid-19[23],[24],[16],[25].
Médicaments[modifier | modifier le code]

En date de juillet 2021, aux États-Unis, le remdesivir est approuvé par le NIH pour certains patients atteints de Covid-19 et il existe des autorisations d'utilisation d'urgence pour le baricitinib, le bamlanivimab, le bamlanivimab / étesevimab et le casirivimab/imdevimab[26]. Dans l'Union européenne, l'utilisation de la dexaméthasone et du remdesivir sont approuvés[27].
Plusieurs médicaments antiviraux sont à l'étude pour la Covid-19, mais aucun ne s'est encore avéré clairement efficace sur la mortalité dans les essais cliniques randomisés publiés[28]. L'innocuité et l'efficacité du plasma de convalescence en tant qu'option de traitement nécessite des recherches supplémentaires[29]. D'autres essais examinent si des médicaments existants peuvent être utilisés efficacement contre la réaction immunitaire du corps face à l'infection par le SRAS-CoV-2,[30]. Les recherches sur les traitements potentiels ont débuté en janvier 2020, et plusieurs médicaments antiviraux sont en cours d'essais cliniques[31],[32],[33]. Bien que la mise au point de nouveaux médicaments s'étale dans le temps[34], plusieurs des médicaments testés sont déjà approuvés pour d'autres utilisations ou font déjà l'objet de tests avancés[35]. Des médicaments antiviraux peuvent être essayés chez les personnes atteintes d'une maladie grave[3]. Des volontaires suivis par l'OMS participent à des essais sur l'efficacité et l'innocuité de traitements potentiels[36].
La dexaméthasone démontre des bénéfices cliniques dans le traitement de la Covid-19 chez les patients hospitalisés avec des besoins d'oxygène selon des essais cliniques randomisés[37],[38],[26]. Les inhibiteurs de l'interleukine-6 (Tocilizumab ou Sarilumab) démontrent aussi des bénéfices cliniques chez les patients sévèrement atteints[15],[39],[1]. Les premières recherches suggéraient que le remdesivir raccourcissait la durée de la maladie et diminuait le risque de décès, mais cela n'a pas été confirmé par des études ultérieures[1].
Il a été démontré que le traitement par anticorps monoclonaux bamlanivimab/étesevimab réduisent le nombre d'hospitalisations, de visites aux urgences ou de décès d'environ 60 à 70%. La combinaison des deux médicaments a une autorisation d'utilisation d'urgence de la FDA aux États-Unis. Le REGN-COV2, un double anticorps monoclonal (casirivimab/imdevimab) bénéficie d'autorisations d'utilisation d'urgence dans de nombreux pays et d'une approbation complète au Japon dans le traitement des formes légère à modérée du Covid-19[40]. L'AZD7442, un autre doublet d'anticorps anticorps monoclonaux est le premier traitement à avoir prouvé une efficacité en prophylaxie chez les sujets immunodéprimés ou ne répondant pas au vaccin dans une étude de phase III[41].
En France le traitement par anticorps monoclonaux est indiqué « en curatif dans le traitement du Covid-19, chez des patients hospitalisés nécessitant une oxygénothérapie non invasive (non intubés) et qui n’ont pas développé naturellement leurs propres anticorps (patients séronégatifs), et en prophylaxie pré-exposition ou post-exposition au SARS-COV-2, chez des populations immunodéprimées ne développant pas de réponse immunitaire malgré un schéma de vaccination complet ; pour des populations non éligibles à la vaccination et qui sont à risque de développer des formes graves de Covid-19 »[42].
La prise de médicaments en vente libre comme le paracétamol ou l'ibuprofène[43],[44], la consommation de liquides et le repos peuvent aider à soulager les symptômes[2],[45],[46]. Selon leur gravité, une oxygénothérapie et une perfusion intraveineuse peuvent être nécessaires[47].
Plusieurs traitements ont été étudiés et se sont avérés inefficaces ou dangereux, et leur utilisation n'est donc pas recommandée. Parmi ceux-ci, on note le baloxavir marboxil, le favipiravir, le lopinavir/ritonavir, le ruxolitinib, la chloroquine, l'hydroxychloroquine, l'interféron β-1a et la colchicine[14].
En octobre 2021, le laboratoire Merck commence sa production en même temps qu'il prévoit de faire une demande d'autorisation de mise sur le marché à l'autorité américaine du médicament pour le molnupiravir, une pilule qui selon les tests menés par le laboratoire permettrait de réduire par deux le risque d'hospitalisation et de décès[48],[49].
Assistance respiratoire[modifier | modifier le code]
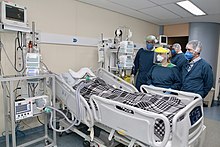
Ventilation mécanique[modifier | modifier le code]
La plupart des cas de Covid-19 ne sont pas suffisamment graves pour nécessiter une ventilation mécanique, mais certains cas sévères en ont besoin[50],[51]. Le type d'assistance respiratoire requis pour les personnes atteintes d'insuffisance respiratoire liée au Covid-19 est activement étudié, avec certaines preuves que l'intubation peut être évitée avec une canule nasale à haut débit ou ventilation non-invasive à pression positive (Bi-Pap)[52]. On ne sait pas lequel est le plus avantageux pour les personnes gravement malades[53]. Certains médecins préfèrent la ventilation mécanique invasive lorsqu'elle est disponible car cette technique limite la propagation des particules d'aérosol par rapport à une canule nasale à haut débit.
Une ventilation mécanique est pratiquée chez 79% des personnes gravement malades hospitalisées, dont 62% ayant précédemment reçu un autre traitement. Parmi elles, 41% sont mortes, selon une étude américaine[54].
Les cas graves sont les plus fréquents chez les personnes âgées de plus de 60 ans, et en particulier de plus de 80 ans[55]. De nombreux pays développés ne disposent pas de suffisamment de lits d'hôpitaux, ce qui limite la capacité de système de santé à gérer une augmentation soudaine du nombre de cas de Covid-19 devant être hospitalisés[56]. Cette capacité limitée est un facteur important derrière les appels à aplatir la courbe de transmission. Une étude en Chine a révélé que 5% des patents ont été admis dans des unités de soins intensifs, 2,3% avaient besoin d'un soutien mécanique de la ventilation et 1,4% étaient décédés[17]. En Chine, environ 30% des personnes hospitalisées pour la Covid-19 sont admises aux soins intensifs[57].
L'administration d'oxyde nitrique inhalé aux personnes ventilées n'est pas recommandée, et les preuves autour de cette pratique sont faibles[58].
Syndrome de détresse respiratoire aiguë[modifier | modifier le code]
La ventilation mécanique devient plus complexe à mesure que le syndrome de détresse respiratoire aiguë (SDRA) se développe dans la Covid-19 car l'oxygénation devient de plus en plus difficile[59]. Des ventilateurs capables de modes de contrôle de pression avec ajustement de la PEP[60] sont nécessaires pour maximiser l'apport d'oxygène tout en minimisant le risque de lésions pulmonaires et de pneumothorax associés au ventilateur par barotraumatisme[61].
Oxygénation par membrane extracorporelle[modifier | modifier le code]
L'oxygénation par membrane extracorporelle (ECMO) est une technologie pulmonaire artificielle utilisée depuis les années 1980 pour traiter l'insuffisance respiratoire et le syndrome de détresse respiratoire aiguë en cas d'échec de la ventilation mécanique conventionnelle. Dans cette procédure complexe, le sang est retiré du corps via de grandes canules, traverse un oxygénateur à membrane qui agit comme un poumon pour distribuer l'oxygène et éliminer le dioxyde de carbone, puis est renvoyé dans le corps. L'organisation ELSO (Extracorporeal Life Support Organization) tient un registre des résultats de cette technologie. Elle a été utilisée chez plus de 120 000 patients dans plus de 435 centres ECMO dans le monde. La mortalité est de 40% pour les patients adultes[62].
L'utilisation initiale de l'ECMO chez les patients avec Covid-19 en Chine au début de la pandémie démontrait des résultats médiocres avec une mortalité de plus de 90%[63]. En mars 2020, le registre ELSO a commencé à collecter des données sur l'utilisation mondiale de l'ECMO pour les patients atteints de Covid-19 et à les afficher sur le site Web ELSO en temps réel. En septembre 2020, les résultats de 1035 patients atteints de Covid-19 pris en charge par l'ECMO de 213 centres expérimentés dans 36 pays différents ont été publiés dans The Lancet et ont démontré une mortalité de 38%, ce qui est similaire à de nombreuses autres maladies respiratoires traitées avec l'ECMO. La mortalité est également similaire à la mortalité de 35% observée dans l'essai EOLIA, le plus grand essai contrôlé randomisé pour l'ECMO dans le SDRA[64]. Ces données de plusieurs centres et plusieurs pays fournissent un support provisoire pour l'utilisation de l'ECMO dans l'insuffisance respiratoire hypoxémique aiguë associée à la Covid-19. Étant donné qu'il s'agit d'une technologie complexe qui peut être gourmande en ressources, des lignes directrices existent pour l'utilisation de l'ECMO pendant la pandémie Covid-19[65],[66],[67].
Prévention de la transmission[modifier | modifier le code]
L'auto-isolement est recommandé pour les personnes atteinte de la Covid-19 ou qui soupçonnent avoir été infectées, incluant celles présentant des symptômes non spécifiques, afin de prévenir la transmission continue du virus et d'aider à Aplatir la courbe de transmission[2]. Dans de nombreuses juridictions, comme le Royaume-Uni, cela est requis par la loi[69]. Les directives sur l'auto-isolement varient d'un pays à l'autre[70],.
Une bonne ventilation, une désinfection adéquate et l'élimination des déchets biologiques sont également essentiels pour limiter la propagation de l'infection[45].
Équipement de protection individuelle[modifier | modifier le code]
Des précautions doivent être prises pour minimiser le risque de transmission du virus, en particulier dans les établissements de soins de santé lors de procédures susceptibles de générer des aérosols, telles l' intubation ou la ventilation par ballon-masque[71]. Pour les professionnels de la santé qui s'occupent de personnes atteintes de Covid-19, le CDC recommande de placer la personne infectée dans une chambre d'isolement à pression négative en plus d'utiliser les précautions standard, les précautions de contact et les précautions contre les particules aériennes[72].
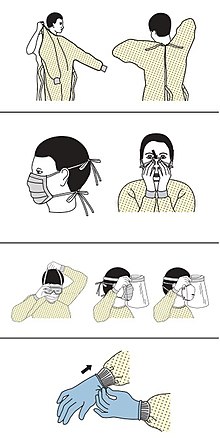
Le CDC offre des lignes directrices pour l'utilisation des équipements de protection individuelle (EPI) pendant la pandémie. L'équipement recommandé est une blouse, un masque de protection ou un masque chirurgical, une protection oculaire et des gants médicaux[73],[74].
Lorsqu'ils sont disponibles, les masques chirurgicaux sont préférables aux masques artisanaux[75]. Le CDC recommande l'utilisation de masques dans les lieux publics, lorsque la distanciation physique n'est pas possible ou lors d'interactions avec des personnes hors de son foyer[76]. Les masques N95 sont approuvés dans les environnements industriels, mais la FDA en a autorisé l'utilisation hospitalière en vertu d'une autorisation d'utilisation d'urgence. Ils sont conçus pour protéger des particules en suspension dans l'air comme la poussière, mais leur efficacité contre un agent biologique spécifique n'est pas garantie[77]. Lorsque les masques médicaux ne sont pas disponibles, le CDC recommande d'utiliser des écrans faciaux ou, en dernier recours, des masques faits maison[78].
Soutien psychologique[modifier | modifier le code]
Les personnes peuvent ressentir de la détresse face à l'isolation, aux restrictions de voyage, aux effets secondaires du traitement ou à la crainte d'être infecté[79],[80]. Le contexte pandémique a aussi des effets collatéraux néfastes sur la santé mentale des populations touchées, notamment chez les jeunes adultes[81].
The Lancet a publié au Royaume-Uni un appel à l'action de 14 pages et a déclaré qu'un éventail de problèmes de santé mentale était susceptible de s'aggraver. La BBC a cité Rory O'Connor en disant : « L'isolement social accru, la solitude, l'anxiété pour la santé, le stress et une récession économique sont une tempête parfaite pour nuire à la santé mentale et au bien-être des gens »[82],[83].
Populations spéciales[modifier | modifier le code]
Traitement concomitant d'autres conditions[modifier | modifier le code]
Au début de la pandémie, des préoccupations théoriques ont été soulevées au sujet des inhibiteurs de l'ECA et des antagonistes des récepteurs de l'angiotensine. Cependant, des recherches ultérieures n'ont trouvé aucune preuve pour justifier l'arrêt de ces médicaments chez les personnes qui les prennent pour des conditions telles que l'hypertension artérielle[16],[84],[85]. Une étude en avril 2020 a révélé que les personnes atteintes de COVID-19 et d'hypertension ont une mortalité toutes causes confondues plus faible lorsqu'elles prennent ces médicaments[86]. Des préoccupations similaires ont été soulevées au sujet des anti-inflammatoires non stéroïdiens (AINS) tels que l'ibuprofène ; celles-ci ne sont pas non plus confirmées, et les AINS peuvent être utilisés pour soulager les symptômes du COVID-19 ou continuer à être utilisés par les personnes qui les prennent pour d'autres conditions[87].
Les personnes qui utilisent des corticostéroïdes topiques ou systémiques pour des affections respiratoires telles que l'asthme ou la bronchopneumopathie chronique obstructive devraient continuer à les prendre comme prescrit même si elles contractent le COVID-19[37].
Pendant la grossesse[modifier | modifier le code]
À ce jour, la plupart des essais cliniques liés au SARS-CoV-2 ont exclu les patientes enceintes ou allaitant, ou en ont inclus seulement quelques-unes. Cette limitation rend difficile la formulation de recommandations thérapeutiques fondées sur des preuves chez ces patientes et limite potentiellement leurs options de traitement contre la Covid-19. Le CDC américain recommande la prise de décision partagée entre le patient et l'équipe clinique lors du traitement des femmes enceintes avec des médicaments expérimentaux[88].
Références[modifier | modifier le code]
- Siemieniuk, Bartoszko, Ge et Zeraatkar, « Drug treatments for covid-19: living systematic review and network meta-analysis », BMJ, BMJ, , m2980 (ISSN 1756-1833, DOI 10.1136/bmj.m2980)
- « Coronavirus » [archive du ], WebMD (consulté le )
- « Q&A: The novel coronavirus outbreak causing COVID-19 », BMC Medicine, vol. 18, no 1, , p. 57 (PMID 32106852, PMCID 7047369, DOI 10.1186/s12916-020-01533-w)
- « Clinical characteristics of novel coronavirus cases in tertiary hospitals in Hubei Province », Chinese Medical Journal, vol. 133, no 9, , p. 1025–1031 (PMID 32044814, PMCID 7147277, DOI 10.1097/CM9.0000000000000744)
- « Comorbidities and multi-organ injuries in the treatment of COVID-19 », Lancet, Elsevier BV, vol. 395, no 10228, , e52 (PMID 32171074, PMCID 7270177, DOI 10.1016/s0140-6736(20)30558-4)
- « Maladie à coronavirus 2019 (COVID-19) : questions-réponses », sur OMS (consulté le ).
- « Unique epidemiological and clinical features of the emerging 2019 novel coronavirus pneumonia (COVID-19) implicate special control measures », Journal of Medical Virology, vol. n/a, no n/a, , p. 568–576 (PMID 32134116, PMCID 7228347, DOI 10.1002/jmv.25748)
- « Could nasal breathing help to mitigate the severity of COVID-19 », Microbes and Infection, vol. 22, nos 4–5, , p. 168–171 (PMID 32387333, PMCID 7200356, DOI 10.1016/j.micinf.2020.05.002)
- « Coronavirus recovery: breathing exercises », www.hopkinsmedicine.org, Johns Hopkins Medicine (consulté le )
- « Review of the 2019 novel coronavirus (SARS-CoV-2) based on current evidence », International Journal of Antimicrobial Agents, vol. 55, no 6, , p. 105948 (PMID 32201353, PMCID 7156162, DOI 10.1016/j.ijantimicag.2020.105948, lire en ligne [archive du ], consulté le )
- « What to Do if You Are Sick » [archive du ], Centers for Disease Control and Prevention (CDC), (consulté le )
- (en) Reed Siemieniuk, Bram Rochwerg, Thomas Agoritsas et François Lamontagne, « A living WHO guideline on drugs for covid-19 », BMJ, vol. 370, , m3379 (ISSN 1756-1833, PMID 32887691, DOI 10.1136/bmj.m3379, lire en ligne, consulté le )
- (en) « Q&A: Dexamethasone and COVID-19 », www.who.int (consulté le )
- (en) « Home », National COVID-19 Clinical Evidence Taskforce (consulté le )
- (en) Pere Domingo, Isabel Mur, Gracia María Mateo et Maria del Mar Gutierrez, « Association Between Administration of IL-6 Antagonists and Mortality Among Patients Hospitalized for COVID-19 », JAMA, (ISSN 0098-7484, DOI 10.1001/jama.2021.11330, lire en ligne, consulté le )
- « COVID-19 Treatment Guidelines », www.nih.gov, National Institutes of Health (consulté le )
- « Clinical Characteristics of Coronavirus Disease 2019 in China », The New England Journal of Medicine, Massachusetts Medical Society, vol. 382, no 18, , p. 1708–1720 (PMID 32109013, PMCID 7092819, DOI 10.1056/nejmoa2002032)
- « COVID-19, ECMO, and lymphopenia: a word of caution », The Lancet. Respiratory Medicine, Elsevier BV, vol. 8, no 4, , e24 (PMID 32178774, PMCID 7118650, DOI 10.1016/s2213-2600(20)30119-3)
- Kim, Read et Fauci, « Therapy for Early COVID-19 », JAMA, American Medical Association (AMA), vol. 324, no 21, , p. 2149 (ISSN 0098-7484, DOI 10.1001/jama.2020.22813)
- (en) « COVID-19 Treatment Guidelines », www.nih.gov, National Institutes of Health (consulté le )/
- (en) Office of the Commissioner, « Coronavirus (COVID-19) Update: FDA Revokes Emergency Use Authorization for Monoclonal Antibody Bamlanivimab », sur FDA, (consulté le )
- Hsu, « Covid-19: What now for remdesivir? », BMJ, BMJ, , m4457 (ISSN 1756-1833, DOI 10.1136/bmj.m4457)
- « Clinical management of COVID-19 », World Health Organization (WHO), (consulté le )
- « Coronavirus (COVID-19) | NICE », National Institute for Health and Care Excellence (consulté le )
- « 2019 Novel coronavirus: where we are and what we know », Infection, vol. 48, no 2, , p. 155–163 (PMID 32072569, PMCID 7095345, DOI 10.1007/s15010-020-01401-y)
- (en) « Therapeutic Management », sur COVID-19 Treatment Guidelines (consulté le )
- (en) European Medicines Agency, « Treatments and vaccines for COVID-19: authorised medicines », European Medicines Agency (consulté le )
- « Pharmacologic Treatments for Coronavirus Disease 2019 (COVID-19): A Review », JAMA, vol. 323, no 18, , p. 1824–1836 (PMID 32282022, DOI 10.1001/jama.2020.6019, lire en ligne
 )
) - Chai, Valk, Piechotta et Kimber, « Convalescent plasma or hyperimmune immunoglobulin for people with COVID-19: a living systematic review », The Cochrane Database of Systematic Reviews, vol. 10, , p. CD013600 (ISSN 1469-493X, PMID 33044747, DOI 10.1002/14651858.CD013600.pub3, lire en ligne)
- « Coronavirus Disease 2019 Treatment: A Review of Early and Emerging Options », Open Forum Infectious Diseases, vol. 7, no 4, , ofaa105 (PMID 32284951, PMCID 7144823, DOI 10.1093/ofid/ofaa105)
- « Chinese doctors using plasma therapy on coronavirus, WHO says 'very valid' approach », Reuters, (lire en ligne, consulté le )
- « With Wuhan virus genetic code in hand, scientists begin work on a vaccine », Reuters, (lire en ligne, consulté le )
- Duddu, « Coronavirus outbreak: Vaccines/drugs in the pipeline for Covid-19 » [archive du ], clinicaltrialsarena.com,
- « Drug treatment options for the 2019-new coronavirus (2019-nCoV) », Bioscience Trends, vol. 14, no 1, , p. 69–71 (PMID 31996494, DOI 10.5582/bst.2020.01020)
- « Therapeutic options for the 2019 novel coronavirus (2019-nCoV) », Nature Reviews. Drug Discovery, vol. 19, no 3, , p. 149–150 (PMID 32127666, DOI 10.1038/d41573-020-00016-0)
- (en) Reuters Staff, « WHO: 'no known effective' treatments for new coronavirus », Reuters, (lire en ligne, consulté le )
- « Australian guidelines for the clinical care of people with COVID-19 », National COVID-19 Clinical Evidence Taskforce, National COVID-19 Clinical Evidence Taskforce (consulté le )
- Rizk, Kalantar-Zadeh, Mehra et Lavie, « Pharmaco-Immunomodulatory Therapy in COVID-19 », Drugs, Springer, vol. 80, no 13, , p. 1267–1292 (ISSN 0012-6667, DOI 10.1007/s40265-020-01367-z)
- « MAGICapp - Making GRADE the Irresistible Choice - Guidelines and Evidence summaries », sur app.magicapp.org (consulté le )
- « Le groupe pharmaceutique suisse Roche a annoncé mardi l'homologation au Japon du cocktail d'anticorps développé avec le laboratoire américain Regeneron pour les formes légère à modérée de Covid-19. », sur Captial,
- (en) « AstraZeneca : Phase III Trial On AZD7442 Meets Primary Endpoint In Preventing COVID-19 », sur nasdaq.com,
- Traitement par anticorps monoclonaux, solidarires-sante.gouv.fr, 24 février 2021
- Covid-19 : non, l’ibuprofène n’aggrave pas l’infection, lepoint et AFP, 8 mai 2021
- Covid-19 : L’ibuprofène est-il réellement dangereux ?, santemagazine, 5 novembre 2020
- « Home care for patients with suspected or confirmed COVID-19 and management of their contacts » [PDF], World Health Organization, (consulté le )
- « Prevention & Treatment » [archive du ], U.S. Centers for Disease Control and Prevention (CDC), (consulté le )
 Cet article reprend du texte de cette source, qui est dans le domaine public.
Cet article reprend du texte de cette source, qui est dans le domaine public. - « Overview of novel coronavirus (2019-nCoV)—Summary of relevant conditions » [archive du ], British Medical Journal (consulté le )
- « Le laboratoire Merck déclare avoir fabriqué la première pilule antivirale contre le Covid-19 », sur L'Obs, (consulté le )
- AFP, « Covid: Merck va demander le feu vert pour une pilule réduisant par deux les hospitalisations », sur Orange Actualités, (consulté le )
- « Care for Critically Ill Patients With COVID-19 », JAMA, vol. 323, no 15, , p. 1499–1500 (PMID 32159735, DOI 10.1001/jama.2020.3633, lire en ligne [archive du ], consulté le )
- World Health Organization, « Clinical management of severe acute respiratory infection when novel coronavirus (2019-nCoV) infection is suspected » [archive du ], (consulté le )
- « The experience of high-flow nasal cannula in hospitalized patients with 2019 novel coronavirus-infected pneumonia in two hospitals of Chongqing, China », Annals of Intensive Care, vol. 10, no 1, , p. 37 (PMID 32232685, PMCID 7104710, DOI 10.1186/s13613-020-00653-z)
- « COVID-19: Respiratory support outside the intensive care unit », The Lancet. Respiratory Medicine, vol. 8, no 6, , p. 538–539 (PMID 32278367, PMCID 7146718, DOI 10.1016/S2213-2600(20)30176-4)
- (en) Cummings, Baldwin, Abrams et Jacobson, « Epidemiology, clinical course, and outcomes of critically ill adults with COVID-19 in New York City: a prospective cohort study », The Lancet, vol. 0, no 10239, , p. 1763–1770 (ISSN 0140-6736, PMID 32442528, PMCID 7237188, DOI 10.1016/S0140-6736(20)31189-2, lire en ligne
 )
) - (en) Srinivas Murthy, Charles D. Gomersall et Robert A. Fowler, « Care for Critically Ill Patients With COVID-19 », JAMA, vol. 323, no 15, , p. 1499 (ISSN 0098-7484, DOI 10.1001/jama.2020.3633, lire en ligne, consulté le )
- (en) Dylan Scott, « Coronavirus is exposing all of the weaknesses in the US health system », sur Vox, (consulté le )
- « Interim Clinical Guidance for Management of Patients with Confirmed Coronavirus Disease (COVID-19) » [archive du ], Centers for Disease Control and Prevention (CDC), (consulté le )
- « Surviving Sepsis Campaign: guidelines on the management of critically ill adults with Coronavirus Disease 2019 (COVID-19) », Intensive Care Med, vol. 46, no 5, , p. 854–887 (PMID 32222812, DOI 10.1007/s00134-020-06022-5)
- « Treatment for severe acute respiratory distress syndrome from COVID-19 », The Lancet. Respiratory Medicine, vol. 8, no 5, , p. 433–434 (PMID 32203709, PMCID 7118607, DOI 10.1016/S2213-2600(20)30127-2)
- « Higher vs lower positive end-expiratory pressure in patients with acute lung injury and acute respiratory distress syndrome: systematic review and meta-analysis », JAMA, vol. 303, no 9, , p. 865–73 (PMID 20197533, DOI 10.1001/jama.2010.218)
- Raiko Diaz et Daniel Heller, Barotrauma And Mechanical Ventilation, StatPearls Publishing, (PMID 31424810, lire en ligne)
- « Extracorporeal Life Support Organization - ECMO and ECLS > Registry > Statistics > International Summary », www.elso.org (consulté le )
- (en) Henry et Lippi, « Poor survival with extracorporeal membrane oxygenation in acute respiratory distress syndrome (ARDS) due to coronavirus disease 2019 (COVID-19): Pooled analysis of early reports », Journal of Critical Care, vol. 58, , p. 27–28 (ISSN 0883-9441, PMID 32279018, PMCID 7118619, DOI 10.1016/j.jcrc.2020.03.011, lire en ligne)
- (en) Combes, Hajage, Capellier et Demoule, « Extracorporeal Membrane Oxygenation for Severe Acute Respiratory Distress Syndrome », New England Journal of Medicine, vol. 378, no 21, , p. 1965–1975 (ISSN 0028-4793, PMID 29791822, DOI 10.1056/NEJMoa1800385, lire en ligne)
- (en) Bartlett, Ogino, Brodie et McMullan, « Initial ELSO Guidance Document: ECMO for COVID-19 Patients with Severe Cardiopulmonary Failure », ASAIO Journal, vol. 66, no 5, , p. 472–474 (ISSN 1058-2916, PMID 32243267, PMCID 7273858, DOI 10.1097/MAT.0000000000001173, lire en ligne)
- (en-US) Shekar, Badulak, Peek et Boeken, « Extracorporeal Life Support Organization Coronavirus Disease 2019 Interim Guidelines: A Consensus Document from an International Group of Interdisciplinary Extracorporeal Membrane Oxygenation Providers », ASAIO Journal, vol. 66, no 7, , p. 707–721 (ISSN 1058-2916, PMID 32358233, PMCID 7228451, DOI 10.1097/MAT.0000000000001193, lire en ligne)
- Ramanathan, Antognini, Combes et Paden, « Planning and provision of ECMO services for severe ARDS during the COVID-19 pandemic and other outbreaks of emerging infectious diseases », The Lancet Respiratory Medicine, vol. 8, no 5, , p. 518–526 (ISSN 2213-2600, PMID 32203711, PMCID 7102637, DOI 10.1016/s2213-2600(20)30121-1, lire en ligne)
- « Sequence for Putting On Personal Protective Equipment (PPE) » [archive du ], Centers for Disease Control and Prevention (CDC) (consulté le )
- « When to self-isolate and what to do - Coronavirus (COVID-19) », NHS, (consulté le )
- « Isolate If You Are Sick », CDC, (consulté le )
- « Staff safety during emergency airway management for COVID-19 in Hong Kong », The Lancet. Respiratory Medicine, vol. 8, no 4, , e19 (PMID 32105633, PMCID 7128208, DOI 10.1016/s2213-2600(20)30084-9)
- « What healthcare personnel should know about caring for patients with confirmed or possible coronavirus disease 2 », Centers for Disease Control and Prevention (CDC), (consulté le )
- « Coronavirus Disease 2019 (COVID-19) » [archive du ], Centers for Disease Control and Prevention (CDC), (consulté le )
- « Coronavirus Disease 2019 (COVID-19) » [archive du ], Centers for Disease Control and Prevention (CDC), (consulté le )
- « Interim Infection Prevention and Control Recommendations for Patients with Suspected or Confirmed Coronavirus Disease 2019 (COVID-19) in Healthcare Settings » [archive du ], Centers for Disease Control and Prevention (CDC), (consulté le )
- (en-US) CDC, « Coronavirus Disease 2019 (COVID-19) », Centers for Disease Control and Prevention, (consulté le )
- « Coronavirus Disease 2019 (COVID-19) Frequently Asked Questions », Food and Drug Administration
- « Strategies for Optimizing the Supply of Facemasks » [archive du ], Centers for Disease Control and Prevention (CDC), (consulté le )
- « Timely mental health care for the 2019 novel coronavirus outbreak is urgently needed », The Lancet. Psychiatry, vol. 7, no 3, , p. 228–229 (PMID 32032543, PMCID 7128153, DOI 10.1016/S2215-0366(20)30046-8)
- « The mental health of medical workers in Wuhan, China dealing with the 2019 novel coronavirus », The Lancet. Psychiatry, vol. 7, no 3, , e14 (PMID 32035030, PMCID 7129673, DOI 10.1016/S2215-0366(20)30047-X)
- CIUSSS Centre-Sud de l'Île de Montréal, « La santé psychologique pendant la pandémie de Covid-19 », sur santemontreal.qc.ca, (consulté le )
- Coronavirus: 'Profound' mental health impact prompts calls for urgent research, BBC, Philippa Roxby, 16 April 2020.
- Multidisciplinary research priorities for the COVID‑19 pandemic: a call for action for mental health science, The Lancet, Emily Holmes, Rory O'Connor, Hugh Perry, et al., 15 April 2020, page 1: "A fragmented research response, characterised by small-scale and localised initiatives, will not yield the clear insights necessary to guide policymakers or the public."
- « Patients taking ACE-i and ARBs who contract COVID-19 should continue treatment, unless otherwise advised by their physician » [archive du ] (consulté le )
- de Simone, « Position Statement of the ESC Council on Hypertension on ACE-Inhibitors and Angiotensin Receptor Blockers » [archive du ], Council on Hypertension of the European Society of Cardiology (consulté le )
- « New Evidence Concerning Safety of ACE Inhibitors, ARBs in COVID-19 », Pharmacy Times (consulté le )
- Research, « FDA advises patients on use of non-steroidal anti-inflammatory drugs (NSAIDs) for COVID-19 », Drug Safety and Availability, (lire en ligne [archive du ], consulté le )
- « Coronavirus Disease 2019 (COVID-19) Treatment Guidelines », CDC, Centers for Disease control and Prevention (consulté le )
 Cet article reprend du texte de cette source, qui est dans le domaine public.
Cet article reprend du texte de cette source, qui est dans le domaine public.
Liens externes[modifier | modifier le code]
Lignes directrices[modifier | modifier le code]
- « JHMI Clinical Recommendations for Available Pharmacologic Therapies for COVID-19 » [PDF], The Johns Hopkins University
- « Bouncing Back From COVID-19: Your Guide to Restoring Movement », The Johns Hopkins School of Medicine
- « Guidelines on the Treatment and Management of Patients with COVID-19 », Infectious Diseases Society of America
- « Coronavirus Disease 2019 (COVID-19) Treatment Guidelines », National Institutes of Health
- OMS. (en) , ((World Health Organization)) Corticosteroids for COVID-19: living guidance, 2 September 2020 (rapport) (hdl 10665/334125)
- OMS. (en) , ((World Health Organization)) Therapeutics and COVID-19: living guideline, 17 December 2020 (rapport), (hdl 10665/337876)
- « Prise en charge clinique des patients ayant la COVID-19 : Lignes directrices provisoires canadiennes », SCSI et AMMI Canada


 French
French Deutsch
Deutsch