Cicatrisation — Wikipédia
La cicatrisation se présente sous deux aspects :
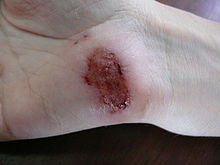
- un phénomène de régénération : on parle alors du processus par lequel se réparent les lésions des tissus et des organes (plaie, brûlures, etc.) ;
- un phénomène de consolidation ou de réconciliation d'éléments auparavant unis et qui avaient été séparés.
On distingue la cicatrisation « de première intention », qui se produit spontanément et rapidement quand les bords de la plaie sont rapprochés ; et la cicatrisation « de seconde intention », dans le cas contraire, qui nécessite un traitement dermatologique (pommade, solution...) ou physique (bistouri, curette...).
Étapes (cas d'une plaie de la peau)[modifier | modifier le code]
Cicatrisation des couches superficielles (atteinte de l'épiderme)[modifier | modifier le code]
Une lésion cutanée est une destruction cellulaire. La cicatrisation se déroule de la manière suivante : en se nécrosant, les cellules libèrent un facteur de croissance épidermique ; sous l'action d'une hormone protéique, les cellules saines de la couche basale épidermique (Stratum germinativum) se divisent et migrent vers la lésion. La migration s'arrête quand la lésion est comblée par de nouvelles cellules. Ces nouvelles cellules se redivisent et reconstituent les différentes couches de l'épiderme.
- Durée : 24 à 48 heures.
- Exemples : coupure, écorchure…
Cicatrisation des couches profondes (atteinte du derme)[modifier | modifier le code]
La cicatrisation est composée de 4 phases qui se chevauchent : l'hémostase, la phase inflammatoire, la phase de prolifération et la phase de remodelage[1].
L'hémostase[modifier | modifier le code]
L'hémostase se met en place dans les heures qui suivent la blessure afin de stopper le saignement. Les vaisseaux lésés vont subir une vasoconstriction et des caillots sanguins vont se former. Les plaquettes, qui sont normalement circulantes, adhèrent à la paroi vasculaire et s'agrègent afin de former le thrombus blanc. Ce dernier va ensuite être remplacé par le thrombus rouge qui est principalement constitué de fibrine. De nombreuses cytokines et facteurs de croissance tels que IL-1, TGFβ, PDGF et EGF sont également relargués, ce qui va induire une cascade de signalisation et permettre la mise en place des phases suivantes en recrutant différents types cellulaires nécessaires à la cicatrisation et notamment les cellules immunitaires[1],[2],[3].
La phase inflammatoire[modifier | modifier le code]
La phase inflammatoire intervient dans les jours qui suivent la lésion et permet d'éliminer les pathogènes et débris cellulaires qui sont présents dans la plaie. Différents signaux sont nécessaire pour que cette phase se mette en place, et notamment des vagues de calcium, un gradient d'espèces réactives de l'oxygène (ROS) et des molécules prurigéniques. Les cellules lésées produisent également des DAMPs, du peroxyde d'hydrogène, des médiateurs lipidiques et des chémokines. Tous ces éléments vont participer au recrutement des cellules immunitaires[1].
Les premières cellules recrutées au site de la plaie sont les neutrophiles. Ils vont éliminer les bactéries et les fragments de tissus dévitalisés par phagocytose, sécréter des peptides anti-microbiens et des facteurs de croissance qui vont permettre l'amplification de la réponse inflammatoire[1].
Ensuite, les monocytes circulants vont être recrutés, se transformer en macrophages pro-inflammatoires de type M1 et vont participer à la phagocytose des pathogènes et débris cellulaires. Ils vont sécréter une seconde vague de facteurs de croissance et cytokines pro-inflammatoires qui vont stimuler la synthèse de collagène, la transformation des fibroblastes en myofibroblastes, l'angiogenèse et la ré-épithélialisation, ce qui va permettre d'initier la phase de prolifération[1].
Les lymphocytes, dernier type cellulaire immunitaire recruté, vont éliminer les neutrophiles par phagocytose afin de progresser vers la phase suivante, mais aussi réguler l'inflammation et stimuler la prolifération des fibroblastes et des kératinocytes[1].
La phase de prolifération[modifier | modifier le code]
Elle est caractérisée par l'activation des kératinocytes, fibroblastes, cellules endothéliales et macrophages afin de refermer la plaie. De nouveaux vaisseaux sanguins vont se former afin de rétablir la circulation sanguine et permettre l'apports de cellules, nutriments et oxygène. Le tissu conjonctif va être réparé. Il est appelé tissu de granulation et est composé principalement de collagène de type I, protéines matricielles et protéoglycans. La matrice extracellulaire est produite majoritairement par les fibroblastes activés, appelés myofibroblastes, qui vont produire le collagène et se contracter afin de participer à la fermeture la plaie. Les macrophages vont switcher vers un phénotype anti-inflammatoire type M2 afin de stopper l'inflammation. Les kératinocytes vont migrer et ré-épithélialiser la plaie afin de reformer un épiderme fonctionnel[1],[2],[3].
La phase de remodelage[modifier | modifier le code]
La phase de remodelage va durer plusieurs mois voire années. Elle est caractérisée par la formation d'une cicatrice et du remodelage de tissu de granulation. Les myofibroblastes vont disparaître, la matrice extracellulaire va être modifiée, notamment le collagène I va être remplacé par le collagène III, et le réseau vasculaire va régresser[1],[2],[3].
Anomalies[modifier | modifier le code]
La cicatrisation peut être gênée par la gravité de la blessure (profondeur, longueur, largeur, propreté, taille et type de la plaie [brûlure, brûlure chimique, coupure, arrachement, etc.]), par la présence d'un corps étranger, d'une infection ou d'une ischémie chronique, par les effets du tabagisme (le tabagisme dit « péri-opératoire est le principal facteur de risque dans l’apparition de troubles de cicatrisation cutanée postopératoire »)[4], par une altération de la réponse au stress (par exemple, chez les sujets âgés, du fait d'une dénutrition ou d'une maladie générale ou d'un traitement immunosuppresseur)[5].
La cicatrisation peut être exubérante et conduire à la formation d'une chéloïde.
À long terme, la peau peut être fragilisée et dépigmentée.
Recherche[modifier | modifier le code]
La cicatrisation naturelle des plaies importantes restaure l'homéostasie de la peau mais sans lui redonner toutes ses fonctionnalités, de même pour la greffe de culture de cellules de peau.
La science médicale recherche donc de nouvelles pistes et stratégies de restauration, si possible rapide, de suture et de cicatrisation. Parmi ces pistes figurent :
- l'ingénierie tissulaire qui peut aller jusqu'à imprimer en 3D des supports provisoires de biomatériaux vivants.
- la thérapie cellulaire, utilisant par exemple des cellules stromales mésenchymateuses (CSM), thérapies encore émergentes, car ces cellules souches isolées de différents tissus peuvent avoir des propriétés distinctes selon leur provenance.
Une étude récente (2020), sur le modèle murin a comparé l'utilisation potentielle des cellules stromales mésenchymateuses (CSM) dérivées du derme (CSD) et des CSM dérivées du tissu adipeux (CSA) avec l'objectif d'améliorer la cicatrisation des plaies cutanées. Des DSC et CSA humains ont été délivrés à des plaies de souris de pleine épaisseur par un échafaudage à base de collagène (Integra Matrix) : les DSC et les CSA ont accéléré et amélioré la cicatrisation, produisant une peau plus similaires à la peau saine[6].
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
- Cicatrice
- Coagulation sanguine
- Hémostase
- Peau
- Épiderme
- Derme
- Tissu conjonctif
- Mélanocyte
- Granulation
Notes et références[modifier | modifier le code]
- (en) Heiko Sorg, « Skin Wound Healing: Of Players, Patterns, and Processes », European Surgical Research,
- Holly N. Wilkinson et Matthew J. Hardman, « Wound healing: cellular mechanisms and pathological outcomes », Open Biology, vol. 10, no 9, , p. 200223 (ISSN 2046-2441, PMID 32993416, PMCID 7536089, DOI 10.1098/rsob.200223, lire en ligne, consulté le )
- Yara Adib, Armand Bensussan et Laurence Michel, « Cutaneous Wound Healing: A Review about Innate Immune Response and Current Therapeutic Applications », Mediators of Inflammation, vol. 2022, , p. 5344085 (ISSN 0962-9351, PMID 35509434, PMCID 9061066, DOI 10.1155/2022/5344085, lire en ligne, consulté le )
- Anouk Rozinthe, Quentin Ode, Fabien Subtil, Michel-Henri Fessy et Jean-Luc Besse, « Influence de l’arrêt du tabagisme sur la cicatrisation après chirurgie du pied et de la cheville », Revue de Chirurgie Orthopédique et Traumatologique, vol. 108, no 7, , p. 877-880 (ISSN 1877-0517, DOI 10.1016/j.rcot.2022.05.021, S2CID 252578405, lire en ligne, consulté le ).
- Mustoe TA, O’Shaughnessy K, Kloeters O, Chronic wound pathogenesis and current treatment strategies: a unifying hypothesis, Plast Reconstr Surg, 2006;117(7 suppl):35S–41S
- Helena Debiazi Zomer, Talita da Silva Jeremias, Buddy Ratner et Andrea Goncalves Trentin, « Mesenchymal stromal cells from dermal and adipose tissues induce macrophage polarization to a pro-repair phenotype and improve skin wound healing », Cytotherapy, (ISSN 1465-3249, DOI 10.1016/j.jcyt.2020.02.003, lire en ligne, consulté le )


 French
French Deutsch
Deutsch