ایزومری سیس–ترانس - ویکیپدیا، دانشنامهٔ آزاد


ایزومری سیس- ترانس، که به عنوان ایزومریسم هندسی یا ایزومریسم پیکربندی نیز شناخته میشود ، اصطلاحی است که در شیمی آلی به کار میرود. پیشوندهای " cis " و " trans " از لاتین گرفته شدهاست: به ترتیب به معنی "یک سو" و "دو سو" است. نشان CIS نشان میدهد که گروه عاملی در یک طرف زنجیره کربن قرار دارند[۱] در حالی که trans بیان میکند که گروه در طرفهای مقابل زنجیره کربن قرار دارند.
ایزومرهای سیس و ترانس هر دو در مولکولهای آلی و در کمپلکسهای کوردینه معدنی رخ میدهند. توصیفهای CIS و ترانس برای مواردی از صورتبندی که در آن دو شکل هندسی به راحتی در هم تنیده میشوند، مانند بیشتر ساختارهای زنجیره باز تک زنجیره ای، مورد استفاده قرار نمیگیرند. در عوض، اصطلاحات " سین " و " أنتی" استفاده میشود. تفاوت های سیس و ترانس:به خاطر وجود پیوند پای توانایی چرخش در فضا را ندارند برای همین سیس و ترانس در حالت طبیعی به هم تبدیل نمیشوند زیرا این کار نیاز به شکستن پیوند پای دارد در نوع قطبیت هم سیس و ترانس با هم متفاوت اند سیس قطبی و ترانس ناقطبی است چگالی سیس از ترانس خود بیشتر بوده و این به این دلیل است که فضاهای خالی کمتری تولید میکند و با توجه به کم بودن حجم چگالی افزایش میابد نقطه جوش سیس از ترانس خود بیشتر بوده و بدین دلیل است که هرچه مولکول قطبی تر باشد نقطه جوش بیشتری را داراست(میدانیم سیس قطبیست) چربی سیس از چربی های غیر اشباع است مثل روغن زیتون ولی ترانس اشباع بوده و برای بدن مضر است مانند چربی های حیوانی (برای همین است که چربی مصرف هر چه کمتر چربی های حیوانی توصیه میشود زیرا در قلب و عروق رسوب میکند) به دلیل سیس بودن روغن زیتون تمایل مایع بودنش بالاست زیرا هر چه مولکول تمایل به قطبیتش بالاتر باشد مایع تر میباشد در ازمایشگاه ها میتوان سیس را به ترانس و برعکس تبدیل کرد برای این کار با برانگیخته کردن الکترون پیوند پای ابتدا ان ها را جدا کرده و سپس بعد از چرخ آن(پیوند سیگما توانایی چرخش را دارد)دوباره الکترون را به آن اضافه میکنند و ایزومر دیگرش را تشکیل میدهند
شیمی آلی[ویرایش]
هنگامی که استخلاف در یک جهت قرار دارند، به دیاسترومر به عنوان cis گفته میشود، در حالی که، هنگامی که استخلاف در جهتهای متضاد باشند، به دیاسترومر عنوان trans گفته میشود. نمونه ای از یک هیدروکربن کوچک که CIS را نمایش میدهد - ایزومریسم ترانس ۲-بوتن است.
ترکیبهای آلیفاتیک حلقوی همچنین میتواند ایزومری سیس - ترانس را نشان دهند. به عنوان نمونه ایزومر هندسی بخاطر ساختار حلقه، ۱٬۲-دی کلروسیکلو هگزان را در نظر بگیرید.
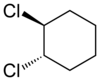 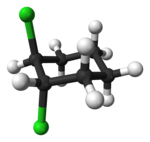 | 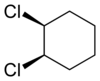  |
| ترانس -۱٬۲-دی کلروسیکلو هگزان | cis -1،۲-دی کلروسیکلو هگزان |
مقایسه ویژگیهای فیزیکی[ویرایش]
ایزومرهای سیس و ترانس اغلب خصوصیات فیزیکی متفاوتی دارند. تفاوت بین ایزومرها، بهطور کلی، ناشی از تفاوت در شکل مولکول یا لحظه دو قطبی کلی است.
 |  |
| cis -2-pentene | ترانس -۲ پنتن |
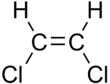 |  |
| CIS -1،۲-دی کلرواتن | ترانس -۱٬۲-دی کلرواتن |
 | 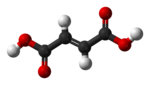 |
| cis- butenioic acid {{سخ}} (اسید مالئیک) | ترانس بوتنیدیو اسید {{سخ}} (اسید فوماریک) |
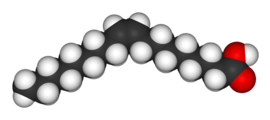 |  |
| اسید اولئیک | اسید الائیدیک |


 French
French Deutsch
Deutsch