Oseltamivir , la enciclopedia libre
| Oseltamivir | ||
|---|---|---|
 | ||
 | ||
| Nombre (IUPAC) sistemático | ||
| (3R,4R,5S)-4-Acetilamino-5-amino-3-(1-etilpropoxi)-1-ciclohexen-1-carboxilato de etilo | ||
| Identificadores | ||
| Número CAS | 196618-13-0 | |
| Código ATC | J05AH02 | |
| PubChem | 65028 | |
| DrugBank | DB00198 | |
| Datos químicos | ||
| Fórmula | C16H28N2O4 | |
| Peso mol. | 312,4 uma | |
| Farmacocinética | ||
| Biodisponibilidad | > 80 %[1] | |
| Unión proteica | 42% (droga parental), 3% (metabolito activo)[1] | |
| Metabolismo | hepático, a GS4071[1] | |
| Vida media | 6-10 h[1] | |
| Excreción | renal a GS4071[1] | |
| Datos clínicos | ||
| Nombre comercial | Tamiflu[2] | |
| Cat. embarazo | B1 (AU) No hay estudios en humanos. El fármaco solo debe utilizarse cuando los beneficios potenciales justifican los posibles riesgos para el feto. Queda a criterio del médico tratante. (EUA) | |
| Estado legal | S4 (AU) POM (UK) ? (EUA) | |
| Vías de adm. | oral | |
Oseltamivir es un profármaco antiviral selectivo contra el virus de la gripe. Lo producen Hoffmann-La Roche en el medicamento de nombre Tamiflu y Procaps con el nombre Tazamir.
Modo de acción[editar]
Su acción se basa en la inhibición de las neuraminidasas presentes en el virus de la influenza. Dichas neuraminidasas son las encargadas de liberar al virus de las células infectadas, y favorecer así su diseminación, estando éstas en el virión. Este compuesto es activo frente a las dos variedades del virus influenza, la A y la B. No modifica la respuesta inmunitaria y humoral contra el virus y otros antígenos no relacionados. Una vez administrado, el oseltamivir disminuye los síntomas de pacientes con la gripe adquirida recientemente, pero no existe evidencia de la eficacia de oseltamivir en otras enfermedades causadas por agentes distintos del virus influenza.[3] Recientemente el BMJ ha publicado un metaanálisis sobre los efectos de los inhibidores de la neuraminidasa.[4]
Se absorbe en su totalidad por vía oral, transformándose en el fármaco (oseltamivir carboxilato) por acción de las esterasas intestinales y hepáticas. Se distribuye fácilmente, pudiéndose encontrar en los pulmones, la membrana pituitaria o mucosa nasal, el oído medio y la tráquea. El máximo de concentración plasmática se da entre 2 y 3 horas tras su ingesta, siendo dicha concentración más de 20 veces superior a la de la prodroga, el oseltamivir. Se estima en un 75% la conversión del oseltamivir al metabolito activo, siendo la concentración proporcional a la dosis.[1]
El metabolito activo no se sigue transformando y se expulsa con la orina (90%) y las heces.
Se deben tomar precauciones cuando se prescriba oseltamivir en sujetos que estén tomando fármacos con un estrecho margen terapéutico y que se eliminan conjuntamente (p.ej. clorpropamida, metotrexato, fenilbutazona). No se han observado interacciones farmacocinéticas entre oseltamivir o su principal metabolito cuando oseltamivir se administra conjuntamente con paracetamol, ácido acetilsalicílico, cimetidina o antiácidos (hidróxidos de aluminio o magnesio y carbonatos cálcicos).[5]
Usos[editar]
Uso en la gripe aviar[editar]
El oseltamivir se ha utilizado ampliamente la epidemia de gripe aviar H5N1 en el sudeste asiático en 2005.[6][7] En respuesta a la epidemia, varios gobiernos, entre los que se incluyen los del Reino Unido, EE. UU. y Australia, han estado almacenando oseltamivir en previsión de una posible pandemia. A pesar de ser cantidades significativas, las cantidades acumuladas no habrían sido suficientes para proteger a toda la población de estos países.[8][9]
A finales de mayo de 2005, la multinacional farmacéutica Roche declaró que la demanda superaba su capacidad de producción, y para intentar satisfacerla Roche planeó la apertura de una nueva planta de producción en EE. UU. durante el segundo semestre de 2005.
En octubre de 2005, la farmacéutica india Cipla anunció que empezaría la fabricación de un fármaco genérico del oseltamivir sin la pertinente licencia de Roche.[cita requerida] Muchas leyes sobre patentes permiten a los gobiernos la cancelación de las restricciones en la fabricación durante emergencias,[cita requerida] a pesar de que Roche ha anunciado su intención de ser la única fabricante. Cipla arguye que puede vender legalmente oseltamivir en la India y otros 49 países en vías de desarrollo, a partir de enero de 2006.[cita requerida] También en octubre, Roche anunció que estaba en negociaciones con cuatro laboratorios farmacéuticos para permitir la fabricación de oseltamivir, incrementando de esta manera la producción.
Gripe A (H1N1)[editar]
El fármaco se utiliza por el momento para combatir la nueva cepa de Influenzavirus A H1N1 de 2009. Se teme que en algún momento el virus se vuelva resistente al oseltamivir. La OMS declaró la pandemia en julio de 2009. En menos de dos meses el virus hizo pie en los cinco continentes (véase Pandemia de gripe A (H1N1) de 2009). No obstante, la tasa de mortalidad calculable a partir del último recuento de casos oficial de la OMS en julio[10] es de un 0.57% sobre 143.841 casos confirmados de infección por el nuevo virus A/H1N1. Dicha tasa es baja en comparación con la habitual en la gripe,[11] y es un 50% inferior a la estimada para la gripe en España en un período de 20 años (1980-1999).[12]
De acuerdo con estudios clínicos y metaanálisis, el tratamiento con los inhibidores de la neuroamidasa provee "pequeños efectos benéficos en el alivio de los síntomas".[13] Oseltamivir ("Tamiflu") y zanamivir ("Relenza") apenas provocan una pequeña reducción en la duración de los síntomas, del orden de 12 horas promedio[14][15] El estudio de Shun-Shin et al concluye:
- Antivirals (oseltamivir and zanamivir) shorten the median duration of influenza by 0.5 to 1.5 days and reduce transmission of influenza by 8%
- Antiviral treatment does not have a clinically significant effect on reducing asthmaexacerbations or on overall use of antibiotics, but oseltamivir is associated with an increased risk of vomiting
- The effects of antivirals on reducing the course of illness or preventing complications in children with the current influenza pandemic are not known but, based on current evidence, might be limited
* Los antivirales (oseltamivir y zanamivir) acortan la duración media de la gripe entre 0,5 y 1,5 días y reducen la transmisión de la gripe en 8%
- El tratamiento con antivirales no tiene un efecto clínico significativo en reducir exacerbaciones asmáticas ni en el uso general de antibióticos, pero el oseltamivir está asociado con un aumento del riesgo de vómitos
- Los efectos de los antivirales en reducir el curso de la enfermedad o evitar complicaciones en niños con la actual pandemia de gripe no se conocen pero, basándonos en la evidencia actual, podrían ser limitados
Shun-Shin, M et al. "Neuraminidase inhibitors for treatment and prophylaxis of influenza in children"[16]
La Organización Mundial de la Salud (OMS) informó el 2 de diciembre de 2009 que se han detectado dos brotes de H1N1 resistente al Tamiflu.[17] Uno en Gales y otro en Carolina del Norte (EE. UU). La nueva mutación del virus -sospechosa de trasmitirse de persona a persona, según la OMS- ha afectado a 12 enfermos. Todos los afectados tenían el sistema inmunitario debilitado.
Reacciones adversas[editar]
Se han reportado los siguientes efectos secundarios tras la toma del fármaco: náuseas, cefalea, bronquitis/bronquitis aguda,[6] infecciones tracto respiratorio insomnio, rinorrea, tos, vértigo, vómitos, dolor abdominal, diarrea, dispepsia, mareo, cansancio, dolor. En niños: vómitos, diarrea, neumonía, sinusitis, bronquitis, otitis media, linfadenopatía, asma (y empeoramiento), epistaxis, náuseas, dolor abdominal, conjuntivitis, trastornos el oído y de la membrana timpánica, dermatitis, rash, eccema, urticaria, edema angioneurótico, reacciones de hipersensibilidad, incluyendo reacciones anafilácticas/anafilactoides, así como casos con una frecuencia rara de trastornos graves de la piel, incluyendo el síndrome de Stevens-Johnson, necrólisis epidérmica tóxica y eritema multiforme. Además, se han notificado trastornos del sistema hepatobiliar, incluyendo hepatitis y aumento de las enzimas hepáticas en pacientes con enfermedad pseudogripal. Estos casos incluyen desde insuficiencia hepática a hepatitis fulminante mortal.[18]
Durante el tratamiento con el fármaco se han notificado convulsiones y trastornos psiquiátricos tales como disminución del nivel de consciencia, alteraciones del comportamiento, alucinaciones y delirio. Estos síntomas también se han presentado en pacientes sin tratamiento.[18] La EMEA no ha establecido ni ha descartado que exista relación entre estos hechos con el consumo de oseltamivir,[19] y aunque en algunos casos se han detectado trastornos psiquiátricos[20] se mantienen las mismas recomendaciones de seguridad con el fármaco.[21]
Controversia sobre posibles efectos neuropsiquiátricos[editar]
Desde su comercialización a gran escala, existe una gran controversia sobre si el oseltamivir pudiera ser causa de efectos adversos neuropsiquiátricos peligrosos, incluidas las autolesiones, en algunos usuarios. Estas manifestaciones han sido estudiadas con más frecuencia en niños que en adultos.[22] Dicha sospecha deriva de los casos reportados en Japón, el país del mundo en el que el medicamento es más ampliamente prescrito. Japón consume el 60% de la producción mundial.[23]
En marzo de 2007, el Ministerio de Salud de Japón advirtió que el oseltamivir no debía administrarse a todos los niños y adolescentes de edad comprendida entre los 10 y los 19 años. Previamente, en mayo de 2004, el Ministerio había decidido cambiar el prospecto que acompaña a oseltamivir para incluir trastornos neuropsiquiátricos entre los posibles efectos adversos, tales como alteración de la conciencia, alteraciones del comportamiento y alucinaciones.[23]
Según el Ministerio de Salud de Japón, entre 2004 y marzo de 2007, quince personas de entre 10 y 19 años, afectados por la gripe aviar y que estaban siendo tratadas con oseltamivir, habían resultado heridas por caer desde edificios, presumiblemente por actos suicidas. En concreto, se describía un caso de un adolescente de 17 años de edad que murió después de saltar delante de un camión.[24]
En abril de 2007, Corea del Sur emitió una advertencia de seguridad restringiendo la prescripción de oseltamivir a los adolescentes salvo en casos especiales.[25]
Una nueva investigación de los datos japoneses se completó en abril de 2007. Se encontró que, desde 2001, 128 pacientes presentaron comportamiento anormal después de tomar oseltamivir. Cuarenta y tres de ellos eran menores de 10 años, 57 pacientes tenían entre 10 y 19 años, y 28 pacientes eran mayores de 20 años. Ocho personas, entre ellos cinco adolescentes y tres adultos, habían muerto por estas acciones.[26]
En octubre de 2006, Shumpei Yokota, profesor de pediatría en la Universidad de Yokohama, había publicado los resultados de las investigaciones realizadas por su departamento con alrededor de 2800 niños, financiadas con 10 millones de yenes por Chugai Pharmaceutical Co. (la farmacéutica que produce oseltamivir en Japón, cuyo 52% es propiedad de Hoffmann-La Roche) a lo largo de cinco años. Sin embargo, estas investigaciones no habían encontrado diferencia alguna entre el comportamiento de los que tomaron oseltamivir y los que no.[27]
Sin embargo, ya en noviembre de 2006, la Food and Drug Administration (FDA) estadounidense modificó la etiqueta de advertencia con el fin de incluir los posibles efectos secundarios neuropsiquiátricos.[28] Esta modificación iba más allá de lo reconocido anteriormente por la FDA, un año antes, justificado porque no había pruebas suficientes para reclamar una relación de causalidad entre el uso de oseltamivir y estos trastornos.[29] El cambio a una postura más cautelosa se atribuyó a 103 nuevos informes de que la FDA recibió, en los que se reportaban delirios, alucinaciones y otras conductas inusuales, sobre todo con pacientes japoneses, recibidas entre el 29 de agosto de 2005 y 6 de julio de 2006. Esto suponía un aumento respecto a los 126 casos similares detectados entre la aprobación del medicamento en 1999 y en agosto de 2005.[30]
Para determinar si se debía levantar la restricción impuesta en 2007, un equipo de investigación del Ministerio de Salud, Trabajo y Bienestar Social de Japón estudió a 10 000 menores de 18 años que habían sido diagnosticado con la gripe desde 2006. El estudio fue finalizado en abril de 2009. Teniendo en cuenta todos los grados de comportamiento anormal, incluidos los menores con problemas de conducta tales como el habla incoherente, el estudio encontró que los niños que tomaron oseltamivir fueron un 54 por ciento más propensos a presentar un comportamiento anormal que aquellos que no tomaron el medicamento. Cuando el equipo limitó su análisis a los niños que habían mostrado un comportamiento anormal que dio lugar a graves lesiones o la muerte, se encontró que aquellos que habían tomado oseltamivir fueron un 25 por ciento más propensos a comportarse de manera inusual.[31]
Por su parte, Roche señala que oseltamivir se ha utilizado para tratar a más de 50 millones de personas desde 1999, y señala que la gripe por sí sola puede causar problemas psicológicos. En marzo de 2007, la Agencia Europea de Medicamentos aseveró que los beneficios de oseltamivir son mayores que los costos, pero que seguía de cerca los informes de seguimiento de Japón.
Comercialización[editar]
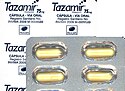
En España y varios países de América Latina el oseltamivir se distribuye en el medicamento con nombre comercial de Tamiflu (Roche), y en Colombia bajo el nombre de Tazamir (Procaps). 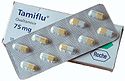
Véase también[editar]
Referencias[editar]
- ↑ a b c d e f Davies, BE (abril de 2010). «Pharmacokinetics of oseltamivir: an oral antiviral for the treatment and prophylaxis of influenza in diverse populations» (PDF). The Journal of Antimicrobial Chemotherapy. 65 Suppl 2: ii5-10. PMC 2835511. PMID 20215135. doi:10.1093/jac/dkq015. Archivado desde el original el 8 de septiembre de 2017.
- ↑ «Tamiflu - Drugs.com». www.drugs.com. Archivado desde el original el 21 de diciembre de 2014. Consultado el 16 de enero de 2017.
- ↑ Vademécum.es, Oseltamivir, advertencias y precauciones
- ↑ Neuraminidase inhibitors for treatment and prophylaxis of influenza in children: systematic review and meta-analysis of randomised controlled trials.BMJ. agosto de 2009
- ↑ Vademécum.es, Oseltamivir fosfato, interacciones
- ↑ a b Jefferson T, Jones MA, Doshi P, Del Mar CB, Hama R, Thompson MJ, Spencer EA, Onakpoya I, Mahtani KR, Nunan D, Howick J, Heneghan CJ (2014). «Neuraminidase inhibitors for preventing and treating influenza in healthy adults and children». Cochrane Database Syst Rev 4 (4): CD008965. PMID 24718923. doi:10.1002/14651858.CD008965.pub4.
- ↑ Jackson, RJ; Cooper, KL; Tappenden, P; Rees, A; Simpson, EL; Read, RC; Nicholson, KG (enero de 2011). «Oseltamivir, zanamivir and amantadine in the prevention of influenza: a systematic review». The Journal of Infection 62 (1): 14-25. PMID 20950645. doi:10.1016/j.jinf.2010.10.003.
- ↑ Farina V, Brown JD. (13 de noviembre de 2006). «"Tamiflu: the supply problem"». Angew Chem Int Ed Engl. (en inglés). 45 (44): 7330-7334. PMID 17051628. doi:10.1002/anie.200602623.
- ↑ Rawat G (May 2013). «Expanding horizons of shikimic acid. Recent progresses in production and its endless frontiers in application and market trends». Appl Microbiol Biotechnol 97 (10): 4277-4287. PMID 23553030. doi:10.1007/s00253-013-4840-y.
- ↑ WHO, Pandemic (H1N1) 2009 - update 58
- ↑ Wilson N, Baker MG. (2009). Eurosurveillance (en inglés). 14 Issue 26.
- ↑ de Mateo S y cols. (2006). Gaceta Sanitaria (en inglés). 20 (1): 67-73.
- ↑ Jefferson T, Demicheli V, Rivetti D, Jones M, Di Pietrantonj C, Rivetti A. (2006). «"Antivirals for influenza in healthy adults: systematic review"». Lancet (en inglés) 367: 303-13.
- ↑ Véase, inter alia, Burch J, Corbett M, Stock C, Nicholson K, Elliot AJ, Duffy S, Westwood M, Palmer S, Stewart L. (2009). «"Prescription of anti-influenza drugs for healthy adults: a systematic review and meta-analysis"». The Lancet Infectious Diseases (en inglés). doi:10.1016/S1473-3099(09)70199-9.
- ↑ Burch J, Paulden M, Conti S, Stock C, Corbett M, Welton N, Ades AE, Sutton A, Cooper N, Elliot AJ, Nicholson K, Duffy S, McKenna C, Stewart L, Westwood M, Palmer S. (2009). «"Antiviral drugs for the treatment of influenza: A Systematic Review and Economic Evaluation."». Health Technology Assessment (en inglés). 13 (58): 1-290. doi:10.3310/hta13580.
- ↑ Shun-Shin M, Thompson M, Heneghan C, Perera R, Harnden A, Mant D. "Neuraminidase inhibitors for treatment and prophylaxis of influenza in children: systematic review and meta-analysis of randomised controlled trials", British Medical Journal 2009; 339:b3172 doi:10.1136/bmj.b3172.
- ↑ Cepa H1N1 resistente al Tamiflu, diario El País, 2 de diciembre de 2009.
- ↑ a b Vademécum.es, Oseltamivir, reacciones adversas
- ↑ Doc. Ref. EMEA/385013/2005 Londres, 17 de noviembre de 2005
- ↑ Updated review of influenza antiviral medicinal products for potential use during pandemic by the Committee for Medicinal Products for Human Use (CHMP) of the European Medicines Agency (EMEA), Doc.Ref.: EMEA/CHMP/592102/2007 Londres, 13 de diciembre de 2007
- ↑ European Medicines Agency recommends no changes for Tamiflu safety information, Doc. Ref.: EMEA/420087/2005 Londres, 15 de diciembre de 2005
- ↑ Waknine, Yael (2006). «Tamiflu May Be Linked to Risk for Self-Injury and Delirium». Medscape. FDA. Consultado el 17 de mayo de 2008.
- ↑ a b Parry, Richard Lloyd (21 de marzo de 2007). «Japan issues Tamiflu warning after child deaths». The Times. Consultado el 5 de mayo de 2009.
- ↑ «Japan to keep stockpiling Tamiflu». Sydney Morning Herald. Reuters. 28 de marzo de 2007. Consultado el 29 de julio de 2009.
- ↑ «SKorea suspends Tamiflu use for young people - official». Forbes. AFX News Limited. 5 de abril de 2007. Archivado desde el original el 4 de junio de 2011. Consultado el 29 de julio de 2009.
- ↑ «Japan finds 128 abnormal cases in Tamiflu probe». Forbes. AFX News Limited. 4 de mayo de 2007. Archivado desde el original el 4 de junio de 2011. Consultado el 29 de julio de 2009.
- ↑ Fuyuno, I. (marzo de 2007). "Tamiflu side effects come under scrutiny" (en inglés). 446 (7134). Nature. ISSN 0028-0836. Archivado desde el original el 24 de julio de 2009. Consultado el 22 de noviembre de 2017.
- ↑ «Flu Drug Tamiflu May Cause Odd Behavior in Children». Forbes. 13 de noviembre de 2006.
- ↑ Pediatric Advisory Committee (2005). Pediatric safety update for Tamiflu (en inglés). Rockville (MD): U.S. Food and Drug Administration.
- ↑ «FDA adds 'abnormal behavior' precaution to Tamiflu label». USA Today. Associated Press. 14 de noviembre de 2006. Consultado el 29 de julio de 2009.
- ↑ «Tamiflu linked to abnormal behaviour». Sydney Morning Herald. Associated Press. 20 de abril de 2009. Consultado el 29 de julio de 2009.
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Oseltamivir.
Wikimedia Commons alberga una categoría multimedia sobre Oseltamivir.- Información del oseltamivir - Biblioteca Nacional de Medicina de EE. UU.
- Sitio oficial de Tamiflu, laboratorios Roche (en inglés)
- Sitio oficial de Tamiflu, laboratorios Roche
- Sitio oficial de PROCAPS
- Stimola AN. Avian Influenza, or "Bird Flu": What You Need to Know. New York, NY, American Council of Science and Health, 2006. Información sobre la gripe aviar. (en inglés)
- Esta obra contiene una traducción parcial derivada de «Oseltamivir» de Wikipedia en inglés, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.


 French
French Deutsch
Deutsch